АЛЬДЕГИДЫ И КЕТОНЫ
АЛЬДЕГИДЫ И КЕТОНЫ – органические соединения, содержащие фрагмент >C=O (углерод, связанный двойной связью с кислородом, его называют карбонильным). У альдегидов карбонильный углерод соединен с атомом Н и органической группой R (общая формула RHC=O), а в кетонах – с двумя органическими группами (общая формула R2С=О).
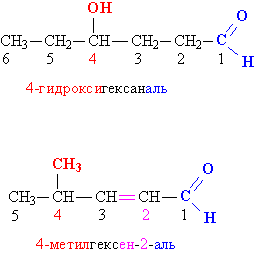
Номенклатура альдегидов и кетонов. Группу –(Н)С=О называют альдегидной, для связывания с органическими группами у нее есть всего одна свободная валентность, это позволяет ей находится только на конце углеводородной цепи (но не в середине). При составлении названия альдегида указывается название соответствующего углеводорода, к которому добавляется суффикс «аль», например, метаналь Н2С=О, этаналь Н3СС(Н)=О, пропаналь Н3ССН2С(Н)=О. В более сложных случаях углеродную цепь группы R нумеруют, начиная с карбонильного углерода, затем с помощью числовых индексов указывают положение функциональных групп и различных заместителей.
Рис. 1. НОМЕНКЛАТУРА АЛЬДЕГИДОВ. Замещающие и функциональные группы, а также соответствующие им цифровые индексы выделены различающимися цветами.
Для некоторых альдегидов часто используют тривиальные (упрощенные) названия, сложившиеся исторически, например, формальдегид Н2С=О, ацетальдегид Н3СС(Н)=О, кротоновый альдегид СН3СН=CHC(H)=O.
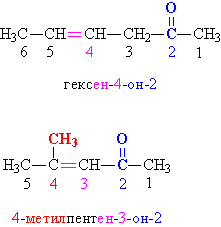
В отличие от альдегидной, кетонная группа >C=O может находиться также в середине углеводородной цепи, поэтому в простых случаях указывают названия органических групп (упоминая их в порядке увеличения) и добавляют слово «кетон»: диметилкетон CH3–CO–CH3, метилэтилкетон CH3CH2–CO–CH3. В более сложных случаях положение кетонной группы в углеводородной цепи указывают цифровым индексом, добавляя суффикс «он». Нумерацию углеводородной цепи начинают с того конца, который находится ближе к кетонной группе (рис. 2).
Рис. 2. НОМЕНКЛАТУРА КЕТОНОВ. Замещающие и функциональные группы и соответствующие им цифровые индексы выделены различными цветами.
Для простейшего кетона CH3–CO–CH3 принято тривиальное название – ацетон.
Химические свойства альдегидов и кетонов
определяются особенностями карбонильной группы >C=O, обладающей полярностью – электронная плотность между атомами С и О распределена неравномерно, сдвинута к более электроотрицательному атому О. В результате карбонильная группа приобретает повышенную реакционную способность, что проявляется в разнообразных реакциях присоединения по двойной связи. Во всех случаях кетоны менее реакционноспособны, чем альдегиды, в частности, из-за пространственных затруднений, создаваемых двумя органическими группами R, наиболее легко участвует в реакциях формальдегид Н2С=О.
1. Присоединение по двойной связи С=О.
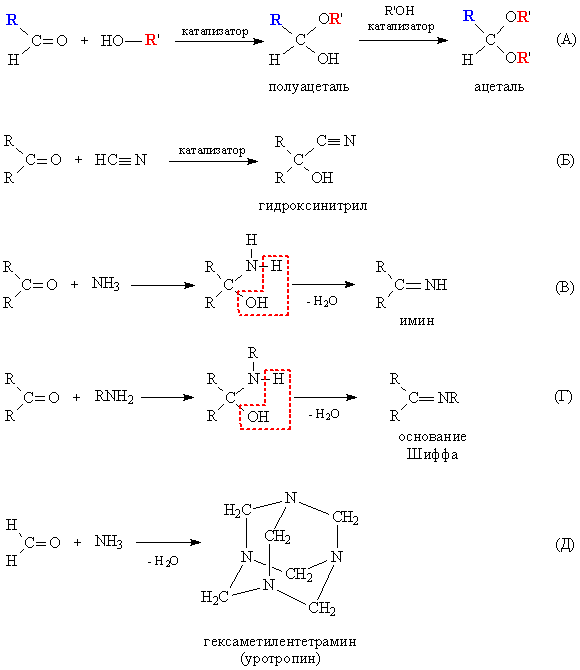
При взаимодействии со спиртами альдегиды образуют полуацетали – соединения, содержащие одновременно алкокси- и гидрокси-группу у одного атома углерода: >C(OH)OR. Полуацетали могут далее реагировать с еще одной молекулой спирта, образуя полные ацетали – соединения, где у одного атома углерода находятся одновременно две RО-группы: >C(OR)2. Реакцию катализируют кислоты и основания (рис. 3А). В случае кетонов присоединение спиртов к двойной связи в С=О затруднено.
Сходным образом альдегиды и кетоны реагируют с синильной кислотой HCN, образуя гидроксинитрилы – соединения, содержащие у одного атома углерода ОН- и CN-группу: >C(OH)CєN (рис. 3Б). Реакция примечательна тем, что позволяет увеличивать углеродную цепь (возникает новая связь С-С).
Точно так же (раскрывая двойную связь С=О) аммиак и амины реагируют с альдегидами и кетонами, продукты присоединения неустойчивы и конденсируются с выделением воды и образованием двойной связи C=N. В случае аммиака получаются имины (рис. 3В), а из аминов образуются так называемые основания Шиффа – соединения, содержащие фрагмент >C=NR (рис. 3Г). Продукт взаимодействия формальдегида с аммиаком несколько иной – это результат циклизации трех промежуточных молекул, в результате получается каркасное соединение гексаметилентетрамин, используемое в медицине как препарат уротропин (рис. 3Д).
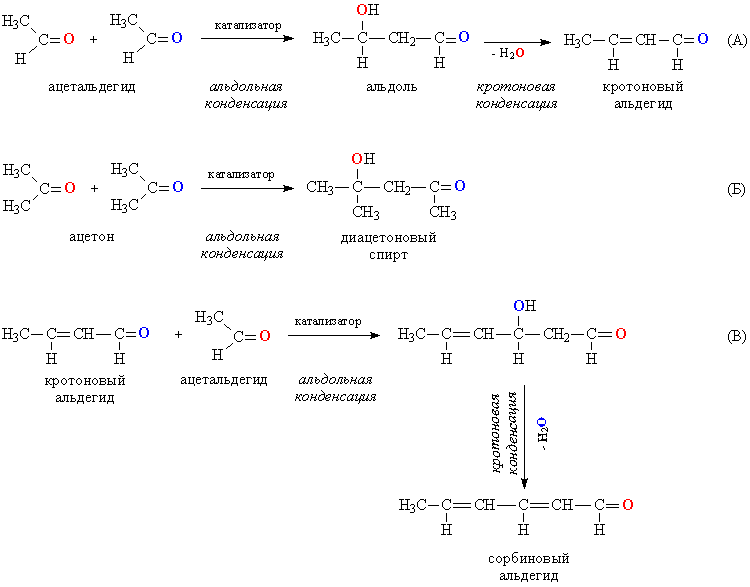
2. Реакции конденсации. Для альдегидов и кетонов возможна конденсация, проходящая между двумя молекулами одного и того же соединения. При такой конденсации альдегидов двойная связь одной из молекул раскрывается, образуется соединение, содержащее одновременно альдегидную и ОН-группу, называемое альдолем (альдегидоспирт). Протекающую конденсацию называют, соответственно, альдольной, эту реакцию катализируют основания (рис. 4А). Полученный альдоль может далее конденсироваться с образованием двойной связи С=С и выделением конденсационной воды. В итоге получается ненасыщенный альдегид (рис. 4А, кротоновой альдегид). Такую конденсацию называют кротоновой по названию первого соединения в ряду ненасыщенных альдегидов. Кетоны также способны участвовать в альдольной конденсации (рис. 4Б), а вторая стадия – кротоновая конденсация, для них затруднена. В альдольной конденсации могут совместно участвовать молекулы различных альдегидов, а также одновременно альдегид и кетон, во всех случаях происходит удлинение углеродной цепи. Получившийся на последней стадии (рис. 4А) кротоновый альдегид, обладая всеми свойствами альдегидов, может далее участвовать в альдольной и кротоновой конденсации при взаимодействии с очередной порцией ацетальдегида, из которого он и был получен (рис. 4В). Таким способом можно удлинять углеводородную цепь, получая соединения, в которых чередуются простые и двойные связи: –СН=СН–СН=СН–.
Конденсация альдегидов и кетонов с фенолами идет с удалением карбонильного атома О (в виде воды), а метиленовая группа СН2 или замещенная метиленовая группа (СНR либо СR2) встраивается между двумя молекулами фенола. Наиболее широко эту реакцию применяют для получения фенолоформальдегидных смол (рис. 5.).
Рис. 5. КОНДЕНСАЦИЯ ФЕНОЛА С ФОРМАЛЬДЕГИДОМ
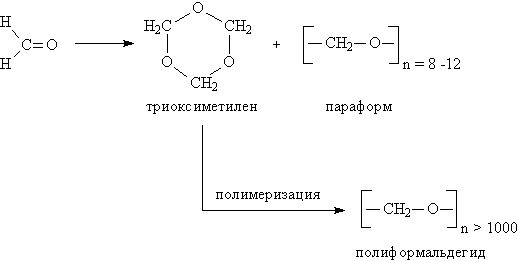
3. Полимеризация карбонильных соединений протекает с раскрытием двойной связи С=О и свойственна, в основном, альдегидам. При упаривании в вакууме водных растворов формальдегида образуется смесь циклических соединений (в основном, триоксиметилен) и линейных продуктов с незначительной длиной цепи n = 8–12 (параформ). Полимеризацией циклического продукта получают полиформальдегид (рис. 6) – полимер с высокой прочностью и хорошими электроизоляционными свойствами, используемый как конструкционный материал в машино- и приборостроении.
Рис. 6. ПРОДУКТЫ ПОЛИМЕРИЗАЦИИ ФОРМАЛЬДЕГИДА
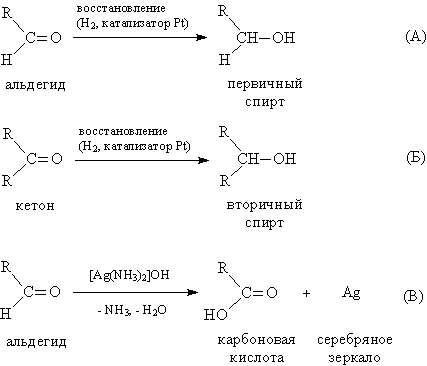
4. Восстановление и окисление. Альдегиды и кетоны представляют собой как бы промежуточные соединения между спиртами и карбоновыми кислотами: восстановление приводит к спиртам, а окисление –- к карбоновым кислотам. При действии Н2 (в присутствии катализатора Pt или Ni) либо других восстанавливающих реагентов, например, LiAlH4, альдегиды восстанавливаются, образуя первичные спирты, а кетоны – вторичные спирты (рис. 7, схемы А и Б).
Окисление альдегидов до карбоновых кислот проходит достаточно легко в присутствии О2 или при действии слабых окислителей, таких как аммиачный раствор гидроксида серебра (рис. 7В). Эта эффектная реакция сопровождается образованием серебряного зеркала на внутренней поверхности реакционного прибора (чаще, обычной пробирки), ее используют для качественного обнаружения альдегидной группы. В отличие от альдегидов, кетоны более устойчивы к окислению, при их нагревании в присутствии сильных окислителей, например, КМnО4, образуются смеси карбоновых кислот, имеющих укороченную (в сравнении с исходным кетоном) углеводородную цепь.
Рис. 7. ВОССТАНОВЛЕНИЕ И ОКИСЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
Дополнительным подтверждением того, что альдегиды занимают промежуточное положение между спиртами и кислотами, служит реакция, в результате которой из двух молекул альдегида получаются спирт и карбоновая кислота (рис. 8А), т.е. одна молекула альдегида окисляется, а другая восстанавливается. В некоторых случаях два полученных соединения – спирт и карбоновая кислота – далее реагируют между собой, образуя сложный эфир (рис.8Б).
Рис. 8. ПРОТЕКАЮЩЕЕ ОДНОВРЕМЕННО ОКИСЛЕНИЕ И ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ
Получение альдегидов и кетонов.
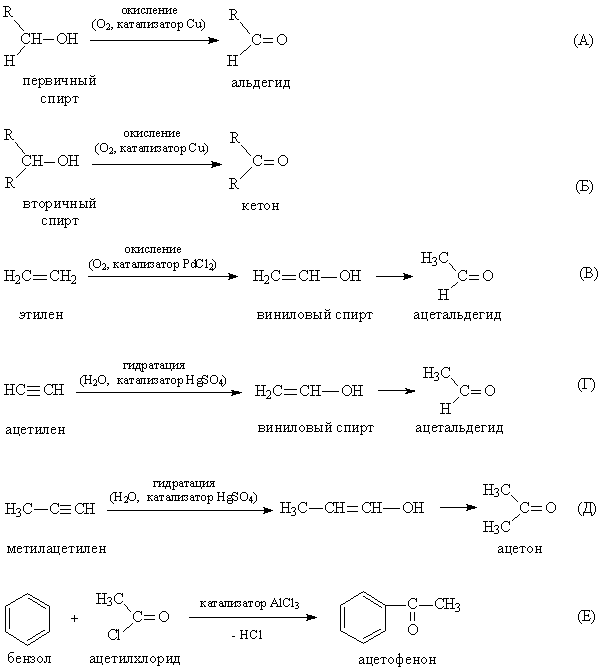
Наиболее универсальный способ – окисление спиртов, при этом из первичных спиртов образуются альдегиды, а из вторичных – кетоны (рис. 9А и Б). Это реакции, обратные реакциям на рис. 7А и Б. Реакция поворачивает «вспять», если изменен действующий реагент (окислитель вместо восстановителя) и катализатор, при окислении спиртов эффективен медный катализатор.
В промышленности ацетальдегид получают окислением этилена (рис. 9В), на промежуточной стадии образуется спирт, у которого ОН-группа «примыкает» к двойной связи (виниловый спирт), такие спирты неустойчивы и сразу изомеризуются в карбонильные соединения. Другой способ – каталитическая гидратация ацетилена (рис. 9Г), промежуточное соединение – виниловый спирт. Если вместо ацетилена взять метилацетилен, то получится ацетон (рис. 9Д). Промышленный способ получения ацетона – окислением кумола. Ароматические кетоны, например, ацетофенон, получают каталитическим присоединением ацетильной группы к ароматическому ядру (рис. 9Е).
Применение альдегидов и кетонов.
Формальдегид Н2С=О (его водный раствор называют формалином) используют как дубитель кожи и консервант биологических препаратов.
Ацетон (СН3)2С=О – широко применяемый экстрагент и растворитель лаков и эмалей.
Ароматический кетон бензофенон (С6Н5)2С=О с запахом герани, используется в парфюмерных композициях и для ароматизации мыла.
Некоторые из альдегидов были сначала найдены в составе эфирных масел растений, а позже искусственно синтезированы.
Алифатический альдегид СН3(СН2)7С(Н)=О (тривиальное название – пеларгоновый альдегид) содержится в эфирных маслах цитрусовых растений, обладает запахом апельсина, его используют как пищевой ароматизатор.
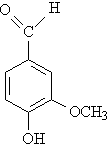
Ароматический альдегид ванилин (рис. 10) содержится в плодах тропического растения ванили, сейчас чаще используется синтетический ванилин – широко известная ароматизирующая добавка в кондитерские изделия (рис. 10).
Рис. 10. ВАНИЛИН
Бензальдегид С6Н5С(Н)=О с запахом горького миндаля содержится в миндальном масле и в эфирном масле эвкалипта. Синтетический бензальдегид используется в пищевых ароматических эссенциях и в парфюмерных композициях.
Бензофенон (С6Н5)2С=О и его производные способны поглощать УФ-лучи, что определило их применение в кремах и лосьонах от загара, кроме того, некоторые производные бензофенона обладают противомикробной активностью и применяются в качестве консервантов. Бензофенон обладает приятным запахом герани, и потому его используют в парфюмерных композициях и для ароматизации мыла.
Способность альдегидов и кетонов участвовать в различных превращениях определила их основное применение в качестве исходных соединений для синтеза разнообразных органических веществ: спиртов, карбоновых кислот и их ангидридов, лекарственных препаратов (уротропин), полимерных продуктов (фенолоформальдегидные смолы, полиформальдегид), в производстве всевозможных душистых веществ (на основе бензальдегида) и красителей.
Михаил Левицкий
Несмеянов А.Н., Несмеянов Н.А. Начала органической химии. М., Химия, 1974
Ответь на вопросы викторины «Неизвестные подробности»