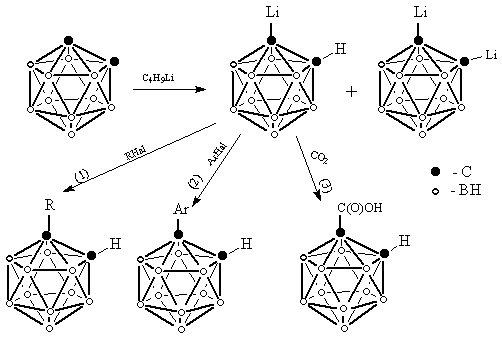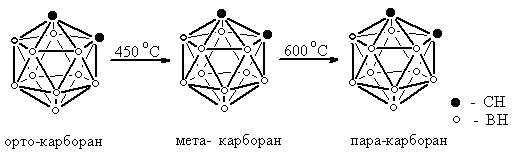КАРБОРАН
КАРБОРАН, более точное название – орто-карборан, борорганическое соединение состава В10Н10С2Н2, бесцветное кристаллическое вещество со слабым камфарным запахом, температура плавления 287–293° С, исключительно устойчиво к действию сильных кислот и оснований, а также окислителей, выдерживает нагревание до 450° С.
Историческая справка.
В 1960-е годы 20 в. возник повышенный интерес к бороводородам (соединениям, содержащим связь В-Н, чаще называемых боранами), которые были привлекательны как вещества, перспективные для создания эффективного ракетного топлива: теплота сгорания бороводородов (~70 кДж/г) много выше, чем углеводородов (45 кДж/г). Недостатком известных к тому моменту различных бороводородов была их крайне низкая стабильность, они легко окислялись кислородом воздуха, и быстро разлагались щелочами и спиртами. Поиски стабильного бороводорода привели к открытию карборана, полученного в 1963 почти одновременно различными группами исследователей.
Открытие карборана по своему масштабу намного перекрыло те практические задачи, которые были поставлены в начале исследований. Появление карборана знаменовало создание новой главы в химической науке и явилось одним из самых заметных событий в химии 20 в.
Синтез и строение карборана.
Получение карборана начинают с трихлорида бора BCl3, который при восстановлении водородом образует диборан В2Н6. Нагревание диборана приводит к образованию каркасного бороводорода В10Н14 (декаборана), который представляет собой заготовку для формирования остова карборана. При взаимодействии декаборана В10Н14, с ацетиленом образуется карборан:
Необходимо иметь в виду, что в показанных выше структурных формулах декаборана и карборна линии, связывающие атомы, не обозначают традиционные валентные связи, в данном случае они использованы для того, чтобы обозначить форму каркаса, в вершинах которого расположены атомы. В бороводородах и в карборане атомы бора и углерода связаны так называемыми трехцентровыми связями, когда связь между тремя атомами осуществляется с помощью двух электронов.
Карборан имеет структуру почти правильного икосаэдра (греческ. eikosi – двадцать, hedra – грань). Это многогранник, собранный из двадцати треугольников, и имеющий двенадцать вершин:
Молекула карборана весьма симметрична, через нее можно провести две плоскости симметрии (плоскость симметрии рассекает объект на две зеркально совпадающие половины). Одна из плоскостей включает в себя линию, связывающую два углеродных атома, вторая плоскость перпендикулярна этой связи.
Химические свойства карборана.
Основное свойство карборана состоит в том, что валентные электроны, связывающие атомы бора и углерода, не принадлежат конкретным атомам, а распределены по всей каркасной молекуле, то есть, делокализованы. Указанное свойство служит основным признаком ароматичности, в данном случае ароматичностью обладает объемная структура, таким образом, карборан представляет собой пример объемной ароматичности. Единая замкнутая электронная система приводит к стабилизации молекулы и является причиной высокой химической устойчивости каркаса.
Электронная плотность в карборане распределена неравномерно. Атомы углерода несут положительный заряд, В результате водород в С-Н – связи приобретает кислый характер и легко замещается щелочным металлом, например, литием, подобно тому, как это происходит в ацетилене. При этом возможно образование как моно -, так и дилитиевые производных. Из них далее могут быть получены различные производные, в которых введенная группа присоединена к атому углерода: алкил- и арилпроизводные (реакции 1, 2), карбоксильные (реакция 3) и многие другие производные. Вся показанная схема фактически представляет собой краткое изложение возможностей органических производных щелочных металлов в органическом синтезе, продемонстрированных в данном случае на примере карборана.
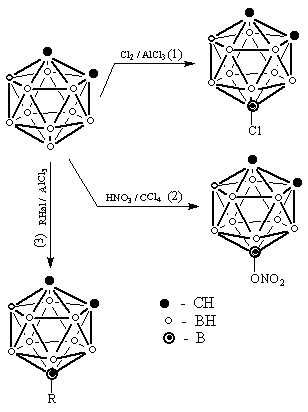
Ароматические свойства карборана наиболее отчётливо проявляются при замещении водорода у атома бора. Ранее было сказано, что положительный заряд сосредоточен на атомах углерода, следовательно, отрицательный заряд и максимальная электронная плотность сосредоточена на атомах бора, наиболее удалённых от углерода, потому замещение при действии реагентов, притягивающихся к отрицательному центру (электрофильных реагентов), обычно проходит именно у этих атомов бора. Так же, как другие ароматические соединения карборан легко галогенируется (реакция 1), нитруется (реакция 2) и алкилируется (реакция 3):
Полученные производные служат основой для получения различных замещенных карборанов с помощью реакций, применяемых в химии ароматических соединений.
«Семейство» карборанов.
Развитие химии карборана привело к появлению большого числа родственных соединений. В настоящее время можно говорить о большом семействе карборанов. Прежде всего, у обсуждаемого нами орто-карборана существует еще два изомера, которые отличаются расположением атомов углерода в структуре каркаса. Они имеют названия, заимствованные у дизамещенных производных бензола: орто -, мета -, и пара-. Из орто - карборана два других изомера образуются при термической перегруппировке:
Получены также карбораны с различным соотношением атомов углерода и бора, имеющие разнообразную форму каркаса:
Из-за сравнительной простоты синтеза и исключительной устойчивости каркаса при различных химических превращениях наиболее изучен орто-карборан.
Некоторые металлы могут встраиваться в карборановый каркас, образуя так называемые гетерокарбораны, при этом атомы металлов оказываются связанными с атомами бора и углерода теми же самыми трехцентровыми связями:
Применение.
Карборан и его производные используют в качестве добавок к твердым ракетным топливам, для получения термостойких полимерных материалов и клеевых композиций, при формировании боруглеродных материалов для солнечных батарей, а также для создания препаратов, используемых при нейтронозахватной терапии при лечении злокачественных опухолей.
Михаил Левицкий
Граймс Р. Карбораны (пер. с англ.), «Мир», Москва, 1974
Леменовский Д.А., Левицкий М.М. Молекулы века, Химия и жизнь, 1999, № 8
Ответь на вопросы викторины «Неизвестные подробности»