ПЕРОКСИДЫ
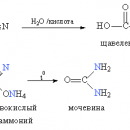
ПЕРОКСИДЫ, соединения, содержащие группировку –О–О–, т.е. производные пероксида водорода Н2О2. Пероксиды металлов образуются при окислении некоторых активных металлов на воздухе, например, при сжигании натрия во влажном воздухе получается Na2O2. Пероксид водорода получают действием холодной серной кислоты на пероксид бария.
После окончания реакции сульфат бария отфильтровывается, вода отгоняется при пониженном давлении; при этом получается 30%-ный водный раствор пероксида водорода, называемый в быту пергидролем или перекисью. Бытовой пероксид водорода содержит 3% Н2О2. Чистый пероксид водорода – сиропообразная голубоватая жидкость. Его водные растворы являются сильными, но медленно действующими окислителями.
Пероксид водорода проявляет также свойства восстановителя в реакциях с более сильными окислителями. Количественно протекающее восстановление перманганата пероксидом водорода является важной аналитической реакцией. Следы пероксида водорода могут определяться с помощью теста с пероксихромовой кислотой. При разложении пероксидов образуются кислород и соответствующий оксид.
Антоновский В.Л., Бузланова М.М. Аналитическая химия органических пероксидных соединений. М., 1978
Вольнов И.И. Перекисные соединения щелочноземельных металлов. М., 1983
Ответь на вопросы викторины «Неизвестные подробности»