ВОДОРОДНАЯ СВЯЗЬ
ВОДОРОДНАЯ СВЯЗЬ (Н-связь) – особый тип взаимодействия между реакционно-способными группами, при этом одна из групп содержит атом водорода, склонный к такому взаимодействию. Водородная связь – глобальное явление, охватывающее всю химию. В отличие от обычных химических связей, Н-связь появляется не в результате целенаправленного синтеза, а возникает в подходящих условиях сама и проявляется в виде межмолекулярных или внутримолекулярных взаимодействий.
Особенности водородной связи.
Отличительная черта водородной связи – сравнительно низкая прочность, ее энергия в 5–10 раз ниже, чем энергия химической связи. По энергии она занимает промежуточное положение между химическими связями и Ван-дер-ваальсовыми взаимодействиями, теми, что удерживают молекулы в твердой или жидкой фазе.
В образовании Н-связи определяющую роль играет электроотрицательность участвующих в связи атомов – способность оттягивать на себя электроны химической связи от атома – партнера, участвующего в этой связи. В результате на атоме А с повышенной электроотрицательностью возникает частичный отрицательный заряд d- , а на атоме-партнере – положительный d+, химическая связь при этом поляризуется: Аd-–Нd+.
Возникший частичный положительный заряд на атоме водорода позволяет ему притягивать другую молекулу, также содержащую электроотрицательный элемент, таким образом, основную долю в образование Н-связи вносят электростатические взаимодействия.
В формировании Н-связи участвуют три атома, два электроотрицательных (А и Б) и находящийся между ними атом водорода Н, структура такой связи может быть представлена следующим образом: Б···Нd+–Аd- (водородную связь обычно обозначают точечной линией). Атом А, химически связанный с Н, называют донором протона (лат. donare – дарить, жертвовать), а Б – его акцептором (лат. acceptor – приемщик). Чаще всего истинного «донорства» нет, и Н остается химически связанным с А.
Атомов – доноров А, поставляющих Н для образования Н-связей, не много, практически всего три: N, O и F, в то же время набор атомов-акцепторов Б весьма широк.
Само понятие и термин «водородная связь» ввели В.Латимер и Р.Родебуш в 1920, для того, чтобы объяснить высокие температуры кипения воды, спиртов, жидкого HF и некоторых других соединений. Сопоставляя температуры кипения родственных соединений Н2O, Н2S, Н2Se, и Н2Te, они обратили внимание на то, что первый член этого ряда – вода – кипит намного выше, чем это следовало из той закономерности, которую образовали остальные члены ряда. Из этой закономерности следовало, что вода должна кипеть на 200°С ниже, чем наблюдаемое истинное значение.
Точно такое же отклонение наблюдается для аммиака в ряду родственных соединений: NН3, Н3P, Н3As, Н3Sb. Его истинная температура кипения (–33° С) на 80° С выше ожидаемого значения.
При кипении жидкости разрушаются только Ван-дер-Ваальсовы взаимодействия, те, что удерживают молекулы в жидкой фазе. Если температуры кипения неожиданно высокие, то, следовательно, молекулы связаны дополнительно еще какими-то силами. В данном случае это и есть водородные связи.
Точно также повышенная температура кипения спиртов (в сравнении с соединениями, не содержащими группу -ОН) – результат образования водородных связей.
В настоящее время надежный способ обнаружить Н-связи дают спектральные методы (чаще всего инфракрасная спектроскопия). Спектральные характеристики групп АН, связанных водородными связями, заметно отличаются от тех случаев, когда такая связь отсутствует. Кроме того, если структурные исследования показывают, что расстояние между атомами Б – Н меньше суммы Ван-дер-Ваальсовых радиусов, то считают, что присутствие Н-связи установлено.
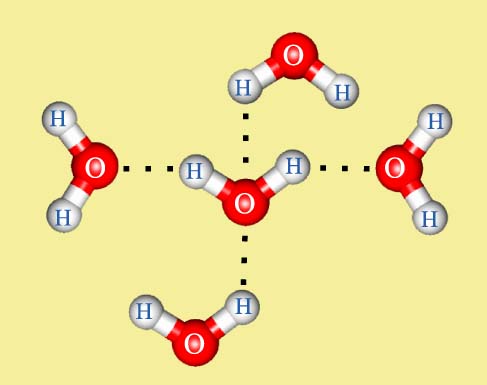
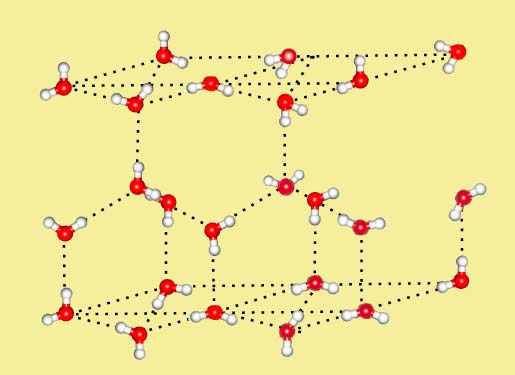
Помимо повышенной температуры кипения водородные связи проявляются себя также при формировании кристаллической структуры вещества, повышая его температуру плавления. В кристаллической структуре льда Н-связи образуют объемную сетку, при этом молекулы воды располагаются таким образом, чтобы атомы водорода одной молекулы были направлены к атомам кислорода соседних молекул:
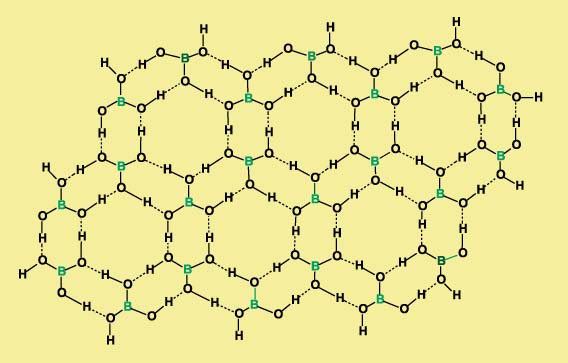
Борная кислота В(ОН)3 имеет слоистую кристаллическую структуру, каждая молекула связана водородными связями с тремя другими молекулами. Упаковка молекул в слое образует паркетный узор, собранный из шестиугольников:
Большинство органических веществ не растворимо в воде, когда такое правило нарушается, то, чаще всего, это результат вмешательства водородных связей.
Кислород и азот – основные доноры протонов, они берут на себя функцию атома А в рассмотренной ранее триаде Б···Нd+–Аd-. Они же, чаще всего, выступают в роли акцепторов (атом Б). Благодаря этому некоторые органические вещества, содержащие O и N в роли атома Б, могут растворяться в воде (роль атома А исполняет кислород воды). Водородные связи между органическим веществом и водой помогают «растащить» молекулы органического вещества, переводя его в водный раствор.
Существует эмпирическое правило: если органическое вещество содержит не более трех атомов углерода на один атом кислорода, то оно легко растворяется в воде:
Бензол весьма незначительно растворим в воде, но если заменить одну группу СН на N, то получим пиридин С5Н5N, который смешивается с водой в любых соотношениях.
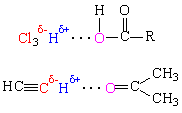
Водородные связи могут проявить себя и в неводных растворах, когда на водороде возникает частичный положительный заряд, а рядом находится молекула, содержащая «хороший» акцептор, как правило кислород. Например, хлороформ HCCl3 растворяет жирные кислоты, а ацетилен HCєCH растворим в ацетоне:
Этот факт нашел важное техническое применение, ацетилен, находящийся под давлением, очень чувствителен к легким сотрясениям и легко взрывается, а его раствор в ацетоне под давлением безопасен в обращении.
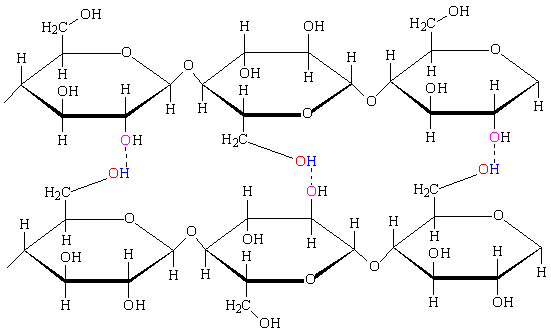
Важную роль играют водородные связи в полимерах и биополимерах. В целлюлозе – основном компоненте древесины – гидроксильные группы, расположены в виде боковых групп полимерной цепи, собранной из циклических фрагментов. Несмотря на сравнительно слабую энергию каждой отдельной Н-связи, их взаимодействие на всем протяжении полимерной молекулы приводит к столь мощному межмолекулярному взаимодействию, что растворение целлюлозы становится возможным лишь при использовании экзотического высокополярного растворителя – реактива Швейцера (аммиачный комплекс гидроксида меди).
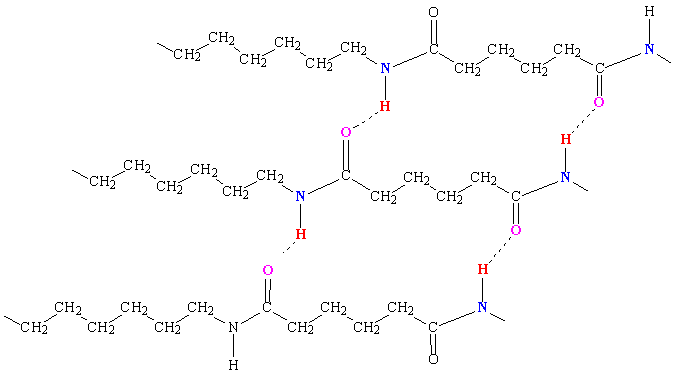
В полиамидах (капрон, нейлон) Н-связи возникают между карбонильными и аминогруппами >С=О···Н–N<, расположенными в соседних полимерных цепях:
Это приводит к образованию кристаллических областей в структуре полимера и увеличению его механической прочности.
То же самое происходит в полиуретанах, имеющих строение, близкое к полиамидам:
-NH-C(O)O-(CH2)4-OC(O)-NH-(CH2)n-NH-C(O)O-
Образование кристаллических областей и последующее упрочнение полимера происходит благодаря образованию Н-связей между карбонильными и аминогруппами >С=О···Н–N<.
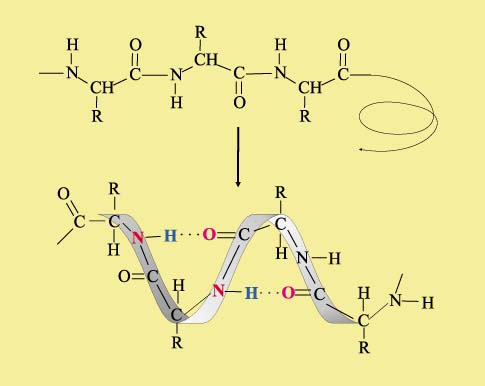
Аналогичным образом происходит объединение параллельно уложенных полимерных цепочек в белках, однако Н-связи предоставляют белковым молекулам также иной способ упаковки – в виде спирали, при этом витки спирали закреплены все теми же водородными связями, возникающими между карбонильной и аминогруппой:
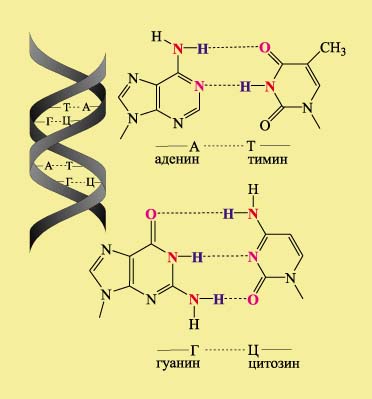
В молекуле ДНК записана вся информация о конкретном живом организме в виде чередующихся циклических фрагментов, содержащих карбонильные и аминогруппы. Таких фрагментов четыре типа: аденин, тимин, цитозин и гуанин. Они расположены в виде боковых подвесков вдоль всей полимерной молекулы ДНК. Порядок чередования этих фрагментов определяет индивидуальность каждого живого существа., При парном взаимодействие карбонильных С=О и аминогрупп NH, а также аминогрупп NH и атомов азота, не содержащих водород, возникают Н-связи, именно они удерживает две молекулы ДНК в форме широко известной двойной спирали:
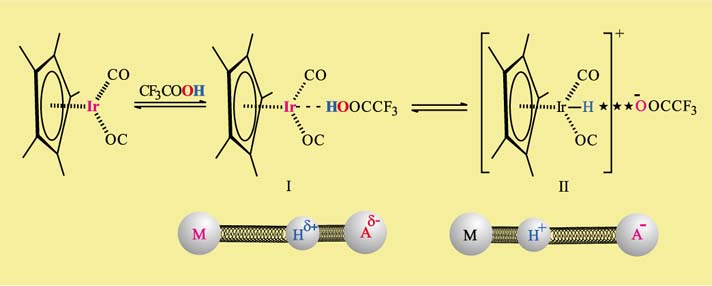
К образованию Н-связи (в роли акцепторов протонов) склонны комплексы некоторых переходных металлов; наиболее расположены к участию в Н-связи комплексы металлов VI–VIII групп. Для того, чтобы такая связь возникла в ряде случае необходимо участие мощного донора протона, например, трифторуксусной кислоты. На первой стадии (см. рисунок ниже) возникает Н-связь с участием атома металла иридия (комплекс I), играющего роль акцептора Б.
Далее при понижении температуры (от комнатной до –50° С) протон переходит к металлу и появляется обычная связь М–Н. Все превращения обратимы, в зависимости от температуры протон может передвигаться либо к металлу, либо к своему донору – аниону кислоты.
На второй стадии металл (комплекс II) принимает протон, а вместе с ним положительный заряд и становится катионом. Образуется обычное ионное соединение (как NaCl). Однако, перейдя к металлу, протон сохраняет свою постоянную тягу к различным акцепторам, в данном случае к аниону кислоты. В результате появляется Н-связь (отмечена звездочками), дополнительно стягивающая ионную пару:
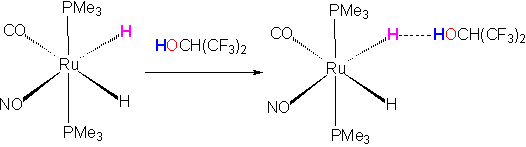
Атом водорода может участвовать в роли атома Б, то есть, акцептора протона в том случае, когда на нем сосредоточен отрицательный заряд, это реализуется в гидридах металлов: Мd+–Нd-, соединениях, содержащих связь металл – водород. Если гидрид металла взаимодействует с донором протона средней силы (например, фторированным трет-бутанолом), то возникает необычный диводородный мостик, где водород сам с собой организует Н-связь: Мd+–Нd-···Нd+–Аd-:
В показанном комплексе клиновидными линиями со сплошной заливкой или поперечной штриховкой обозначены химические связи, направленные к вершинам октаэдра.
Михаил Левицкий
Пиментел Дж., О. Мак-Клеллан. Водородная связь, пер. с англ., М., 1964
Эпштейн Л.М, Шубина Е.С. Многоликая водородная связь. «Природа», 2003, № 1
Ответь на вопросы викторины «Неизвестные подробности»