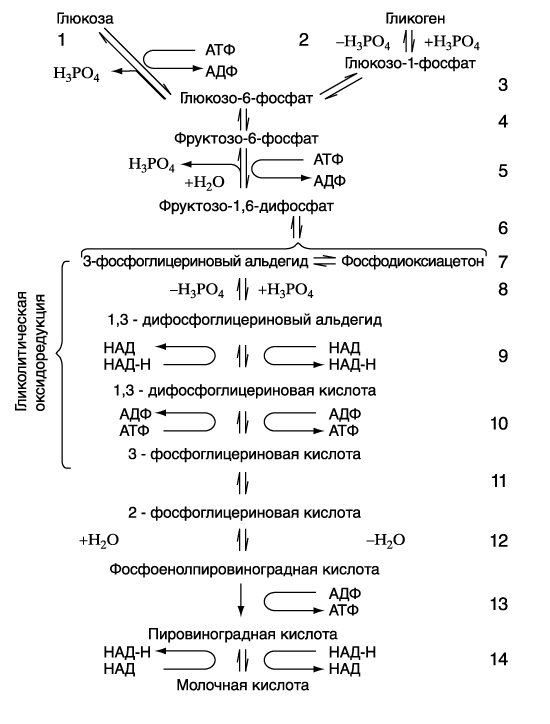
ГЛИКОЛИЗ
ГЛИКОЛИЗ (от греч. glykys – сладкий и lysis – распад, разложение) – один из трех основных (гликолиз, цикл Кребса и путь Энтнера – Дудорова) способов выработки энергии в живых организмах. Это процесс анаэробного (т.е. не требующего участия свободного О2) ферментативного негидролитического расщепления углеводов (главным образом глюкозы и гликогена) в животных тканях, сопровождающийся синтезом аденозинтрифосфорной кислоты (АТФ) и заканчивающийся образованием молочной кислоты. Гликолиз важен для мышечных клеток, сперматозоидов, растущих тканей (в том числе, опухолевых), т.к. обеспечивает накопление энергии в отсутствие кислорода. Но известен и гликолиз в присутствии О2 (аэробный гликолиз) – в эритроцитах, сетчатке глаза, тканях плода сразу после рождения и в слизистой оболочке кишечника. В изучение гликолиза большой вклад внесли Г. и К.Кори, а также такие пионеры биохимии как О.Мейерхоф и Г.Эмбден. Гликолиз был первой до конца расшифрованной последовательностью биохимических реакций (с конца 19 в. по 1940-е). Гексозомонофосфатный шунт или пентозофосфатный путь в некоторых клетках (эритроциты, жировая ткань) также может играть роль поставщика энергии.
Кроме глюкозы, в процесс гликолиза могут вовлекаться глицерин, некоторые аминокислоты и др. субстраты. В мышечной ткани, где основной субстрат гликолиза – гликоген, процесс начинается с реакций 2 и 3 (см. схему) и носит название гликогенолиза. Общим промежуточным продуктом для гликогенолиза и гликолиза является глюкозо-6-фосфат. Обратный путь образования гликогена называется гликогенезом.
Продукты, образующиеся при гликолизе, являются субстратами последующих окислительных превращений (см. Трикарбоновых кислот цикл или цикл Кребса). Процессами, аналогичными гликолизу, являются молочнокислое, маслянокислое, спиртовое, глицериновое брожение, протекающее в растительных, дрожжевых и бактериальных клетках. Интенсивность отдельных стадий гликолиза зависит от кислотности – водородного показателя – рН (оптимум рН 7–8), температуры и ионного состава среды. Последовательность реакций гликолиза (см. схему) хорошо изучена и промежуточные продукты идентифицированы. Растворимые ферменты гликолиза, присутствующие в клеточном соке, выделены в кристаллическом или очищенном виде.
Ферменты, осуществляющие отдельные этапы гликолиза:
1. Гексокиназа КФ2.7.1.1 (или глюкокиназа КФ2.7.1.2)
2. Гликогенфосфорилаза КФ2.4.1.1
3. Фосфоглюкомутаза КФ2.7.5.1
4. Глюкозофосфатизомераза КФ5.3.1.9
5. Фосфофруктокиназа КФ2.7.1.11
6. Фруктозобисфосфатальдолаза КФ4.1.2.13
7. Триозофосфатизомераза КФ5.3.1.1
8, 9. Глицеральдегидфосфатдегидрогеназа КФ1.2.1.12
10. Фосфоглицераткиназа КФ2.7.2.3
11. Фосфоглицеромутаза КФ2.7.5.3
12. Енолаза КФ4.2.1.11
13. Пируваткиназа КФ2.7.1.40
14. Лактатдегидрогеназа КФ1.1.1.27
Гликолиз начинается с образования фосфорных производных сахаров, что способствует превращению циклической формы субстрата в ациклическую, более реакционноспособную. Одной из реакций, регулирующих скорость гликолиза, является реакция 2, катализируемая ферментом фосфорилазой. Центральная регуляторная роль в гликолизе принадлежит ферменту фосфофруктокиназе (реакция 5), активность которой тормозится АТФ и цитратом, но стимулируется продуктами ее распада. Центральным звеном гликолиза является гликолитическая оксидоредукция (реакции 8–10), представляющая собой окислительно-восстановительный процесс, протекающий с окислением 3-фосфоглицеринового альдегида до 3-фосфоглицериновой кислоты и восстановлением кофермента никотинамидадениндинуклеотида (НАД). Эти превращения осуществляет дегидрогеназа 3-фосфоглицеринового альдегида (ДФГА) при участии фосфоглицераткиназы. Это – единственный окислительный этап в гликолизе, но и он не требует свободного кислорода, необходимо лишь присутствие НАД+, который при этом восстанавливается до НАД-Н2.
В результате оксидоредукции (окислительно-восстановительный процесс) высвобождается энергия, аккумулирующаяся (в виде богатого энергией соединения АТФ) в процессе субстратного фосфорилирования. Второй реакцией, обеспечивающей образование АТФ, является реакция 13 – образование пировиноградной кислоты. В анаэробных условиях гликолиз кончается образованием молочной кислоты (реакция 14) под действием лактатдегидрогеназы и с участием восстановленного НАД, который при этом окисляется до НАД (НАД-Н2) и вновь может быть использован на окислительном этапе. В аэробных условиях пировиноградная кислота окисляется в митохондриях в ходе цикла Кребса.
Т.о., при расщеплении 1 молекулы глюкозы образуются 2 молекулы молочной кислоты и 4 молекулы АТФ. В то же время на первых стадиях гликолиза (см. реакции 1, 5) затрачиваются 2 молекулы АТФ на 1 молекулу глюкозы. В процессе гликогенолиза образуется 3 молекулы АТФ, т.к. не нужно тратить АТФ для получения глюкозо-6-фосфата. Первые девять реакций гликолиза представляют собой его эндергоническую (с поглощением энергии) фазу, а последние реакции – экзергоническую (с выделением энергии) фазу. В процессе гликолиза выделяется только около 7% теоретической энергии, которая может быть получена при полном окислении глюкозы (до СО2 и Н2О). Однако общая эффективность накопления энергии в форме АТФ составляет 35–40%, а в практических условиях клетки может быть и выше.
Глицеральдегидфосфатдегидрогеназа и лактатдегидрогеназа внутренне сопряжены (один требует НАД+, другой образует НАД+), что обеспечивает круговорот этого кофермента. В этом, возможно, заключается основное биохимическое значение терминальной дегидрогеназы.
Все реакции гликолиза обратимы, кроме 1, 5 и 13. Однако можно получить глюкозу (реакция 1) или фруктозомонофосфат (реакция 5) из их фосфорных производных при гидролитическом отщеплении фосфорной кислоты в присутствии соответствующих ферментов; реакция 13 практически необратима, по-видимому, вследствие высокой энергии гидролиза фосфорной группировки (около 13 ккал/моль). Поэтому образование глюкозы из продуктов гликолиза идет другим путем.
В присутствии O2 скорость гликолиза снижается (эффект Пастера). Есть примеры подавления гликолизом тканевого дыхания (эффект Кребтри) в некоторых интенсивно гликолизирующих тканях. Механизмы взаимоотношений анаэробных и аэробных окислительных процессов до конца не изучены. Одновременное регулирование процессов гликолиза и гликогенеза однозначно определяет поток углерода по каждому из этих путей в зависимости от нужд организма. Контроль осуществляется на двух уровнях – гормональном (у высших животных через регуляторные каскады с участием вторичных посредников) и метаболическом (у всех организмов).
Игорь Рапанович
Кнорре Д.Г., Мызина С.Д. Биологическая химия. М., Высшая школа, 2003
Кольман Я., Рем К.-Г. Наглядная биохимия. М., Мир, 2004
Ответь на вопросы викторины «Неизвестные подробности»