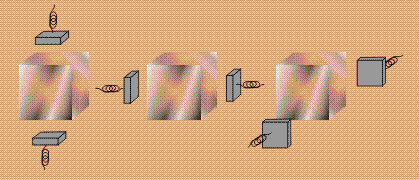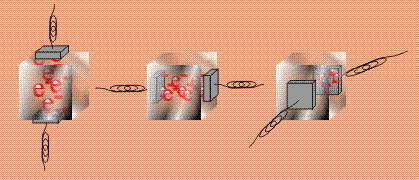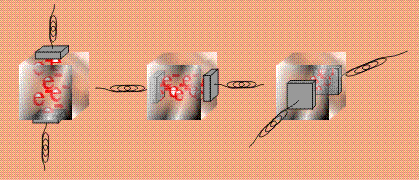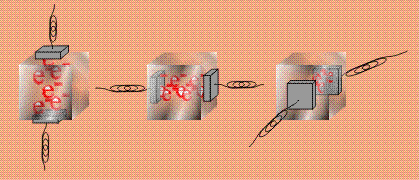ОРГАНИЧЕСКИЕ МЕТАЛЛЫ
ОРГАНИЧЕСКИЕ МЕТАЛЛЫ – общепринятое образное название соединений, не содержащих атомов металлов и, в то же время, обладающих электропроводимостью металлического типа. Металлическая (или электронная) проводимость осуществляется за счет перемещения электронов, в отличие от растворов электролитов, где перемещаются ионы.
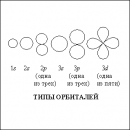
Органические металлы получают на основе соединений, содержащих чередующиеся простые и двойные связи, а также атомы, содержащие неподеленные электронные пары (S, N). Именно такое сочетание компонентов позволяет в некоторых случаях получить молекулы с подвижной объединенной оболочкой из р-электронов.
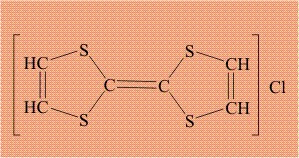
Соединение, состоящее из двух серусодержащих циклов, соединенных двойной связью (тиофульвален), легко образует комплекс с элементарным хлором:
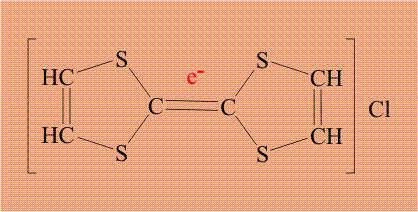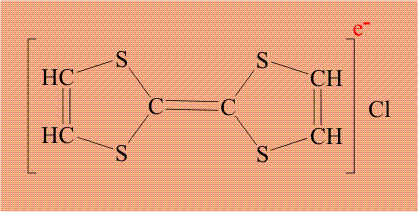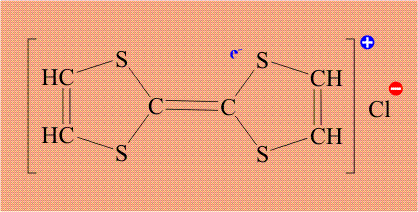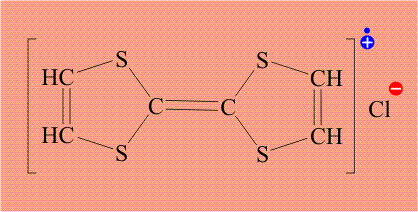
Поскольку хлор необычайно склонен дополнять свою электронную оболочку до 8 электронов, он забирает электрон (отмечен красным цветом) у тиофульвалена, при этом хлор становится анионом, а тиофульвален катионом: По существу, это процесс внутримолекулярного окисления – восстановления.
Тиофульвален имеет единую, легко подвижную электронную оболочку, поэтому электрон уходит не с конкретного атома, а со всей молекулы целиком. Кроме того, в исходном тиофульвалене все электроны были спарены, удаление одного электрона приводит к тому, что в молекуле появляется электрон без пары (отмечен синим цветом). Органическую молекулу, содержащую неспаренный электрон, называют радикалом, и такой электрон обозначают точкой. В итоге, молекула тиофульвалена становится и катионом и радикалом одновременно, общепринятое название «катион-радикал», который обозначают точкой (неспаренный электрон) и знаком «плюс» (катион):
Возникший неспаренный электрон также принадлежит не конкретному атому, а всей молекуле целиком, то есть, он делокализован и потому может легко перемещаться. Именно эти электроны, находящиеся в массе вещества, обеспечивает электропроводимость, таким образом, задача атома хлора – создать неспаренный электрон у тиофульвалена. Проводимость в полученном комплексе довольно необычна.
Все металлы обладают так называемой трехмерной проводимостью: если взять кубик из железа и прикладывать электроды к любым парам противоположных граней, то проводимость будет наблюдаться всегда, ток может идти в любом направлении (кубики условно показаны полупрозрачными):
В кристалле молекулы тиофульвалена располагаются параллельно друг другу, образуя пакеты. Проводимость наблюдается только вдоль этих пакетов, в другом направлении ток не проходит, такую проводимость называют одномерной:
В настоящее время известно несколько десятков комплексов подобного типа, у некоторых из них проводимость почти такая, как у железа, а отдельные представители при понижении температуры способны переходить в сверхпроводящее состояние. В перспективе намечено использовать органические металлы в качестве неметаллических проводников в электронике, а также в роли электродов в химических источниках тока.
М.М.Левицкий
Жуховицкий В.Б., Хидекель М.Л., Дюмаев К.М. – журнал «Успехи химии», 1985, т. 54, выпуск. 2
Левицкий М.М. – Эстетическая химия. В журнале «Химия. Методика преподавания в школе», 2003, №5
Ответь на вопросы викторины «Неизвестные подробности»