МАГНИЙ
МАГНИЙ (Magnesium) Mg, химический элемент 2-й (IIa) группы Периодической системы. Атомный номер 12, относительная атомная масса 24,305. Природный магний состоит из трех природных изотопов 24Mg (78,60%), 25Mg (10,11%) и 26Mg (11,29%). Степень окисления +2, очень редко +1.
История открытия элемента.
Соединения магния были известны человеку очень давно. Магнезитом (по-гречески Magnhsia oliqV) называли мягкий белый, мылкий на ощупь минерал (мыльный камень, или тальк), который находили в районе Магнезии в Фессалии. При прокаливании этого минерала получали белый порошок, который стали именовать белой магнезией.
В 1695 Н.Гро, выпаривая минеральную воду Эпсомского источника (Англия), получил соль, обладавшую горьким вкусом и слабительным действием (MgSO4·7H2O). Спустя несколько лет выяснилось, что при взаимодействии с содой или поташом эта соль образует белый рыхлый порошок, такой же, какой образуется при прокаливании магнезита.
В 1808 английский химик и физик Гемфри Дэви при электролизе слегка увлажненной белой магнезии с окисью ртути в качестве катода получил амальгаму нового металла, способного образовывать белую магнезию. Его назвали магнием. Дэви получил загрязненный металл, а чистый магний был выделен лишь в 1829 французским химиком Антуаном Бюсси (Bussy Antoine) (1794–1882).
Распространение магния в природе и его промышленное извлечение.
Магний есть в кристаллических горных породах в виде нерастворимых карбонатов или сульфатов, а также (в менее доступной форме) в виде силикатов. Оценка его общего содержания существенно зависит от используемой геохимической модели, в частности, от весовых отношений вулканических и осадочных горных пород. Сейчас используются значения от 2 до 13,3%. Возможно, наиболее приемлемым является значение 2,76%, которое по распространенности ставит магний шестым после кальция (4,66%) перед натрием (2,27%) и калием (1,84%).
Большие области суши, такие как Доломитовые Альпы в Италии состоят преимущественно из минерала доломита MgCa(CO3)2. Там встречаются и осадочные минералы магнезит MgCO3, эпсомит MgSO4·7H2O, карналлит K2MgCl4·6H2O, лангбейнит K2Mg2(SO4)3.
Залежи доломита есть во многих других районах, в том числе в Московской и Ленинградской областях. Богатые месторождения магнезита найдены на Среднем Урале и в Оренбургской области. В районе г.Соликамска разрабатывается крупнейшее месторождение карналлита. Силикаты магния представлены базальтовым минералом оливином (Mg,Fe)2(SiO4), мыльным камнем (тальк) Mg3Si4O10(OH)2, асбестом (хризотил) Mg3Si2O5(OH)4 и слюдой. Шпинель MgAl2O4 относится к драгоценным камням.
Большое количество магния содержится в водах морей и океанов и в природных рассолах (см. ХИМИЯ ГИДРОСФЕРЫ). В некоторых странах именно они являются сырьем для получения магния. По содержанию в морской воде из металлических элементов он уступает только натрию. В каждом кубометре морской воды содержится около 4 кг магния. Магний есть и в пресной воде, обусловливая, наряду с кальцием, ее жесткость.
Магний всегда содержится в растениях, так как входит в состав хлорофиллов.
Характеристика простого вещества и промышленное получение металлического магния.
Магний – серебристо-белый блестящий металл, сравнительно мягкий, пластичный и ковкий. Его прочность и твердость минимальны по распространенности для литых образцов, выше – для прессованных.
В обычных условиях магний устойчив к окислению за счет образования прочной оксидной пленки. Вместе с тем он активно реагирует с большинством неметаллов, особенно при нагревании. Магний воспламеняется в присутствии галогенов (при наличии влаги), образуя соответствующие галогениды, и горит ослепительно ярким пламенем на воздухе, превращаясь в оксид MgO и нитрид Mg3N2:
2Mg(к) + O2(г) = 2MgO(к); DG° = –1128 кДж/моль
3Mg(к) + N2(т) = Mg3N2(к); DG° = –401 кДж/моль
Несмотря на невысокую температуру плавления (650° С), расплавить магний на воздухе невозможно.
При действии водорода под давлением 200 атм при 150° С магний образует гидрид MgH2 . С холодной водой магний не реагирует, но из кипящей воды вытесняет водород и образует гидроксид Mg(OH)2:
По окончании реакции величина рН (10,3) образовавшегося насыщенного раствора гидроксида магния отвечает равновесию:
Mg(OH)2(т) 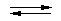 Mg2+ + 2OH–; ПР = 6,8·10–12
Mg2+ + 2OH–; ПР = 6,8·10–12
Оксидная пленка на поверхности магния не устойчива в слабокислотной среде, поэтому магний разрушается под действием горячего концентрированного раствора хлорида аммония:
Mg + 2NH4Cl = MgCl2 + 2NH3– + H2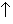
При действии водяного пара продуктами являются оксид или гидроксид магния и водород.
Магний легко реагирует с кислотами, давая соответствующие соли:
Холодные концентрированные азотная и серная кислоты пассивируют магний. Он устойчив также к действию фтороводорода и фтороводородной кислоты благодаря образованию защитной пленки фторида магния.
Аммиак взаимодействует с магнием при повышенной температуре с образованием нитрида магния. Метанол реагирует с магнием при 200° С с образованием метилата магния Mg(OMe)2, а этанол (активированный следовыми количествами иода) взаимодействует подобным образом уже при комнатной температуре. Алкил- и арилгалогениды RX вступают в реакцию с магнием с образованием реактивов Гриньяра RMgX.
Магний производится в больших количествах электролизом расплава смеси хлоридов магния, калия и натрия или кремнийтермическим восстановлением. Для электролитического процесса используется или расплавленный безводный хлорид магния MgCl2 (при 750° С), или (при несколько более низкой температуре) частично гидратированный хлорид магния, выделенный из морской воды. Содержание хлорида магния в расплаве составляет 5–8%. При снижении концентрации уменьшается выход магния по току, а при ее повышении – увеличивается расход электроэнергии. Процесс идет в специальных ваннах-электролизерах. Расплавленный магний всплывает на поверхность ванны, откуда его время от времени выбирают вакуум-ковшом и затем разливают по формам.
Полученный магний, содержащий около 0,1% примесей, очищают переплавкой с флюсами, зонной плавкой или возгонкой в вакууме.
В кремнийтермическом процессе используется прокаленный доломит и ферросилиций при пониженном давлении и температуре 1150° С. В качестве восстановителя применяют также карбид кальция при 1280–1300° С (карбидотермический способ) или углерод выше 2100° С (карбидотермический способ):
В последнем случае образующую смесь монооксида углерода и паров магния необходимо быстро охлаждать инертным газом для предотвращения обратной реакции.
Мировое производство магния приближается к 400 тыс. т в год. Главными производителями являются США (43%), страны СНГ (26%) и Норвегия (17%). В последние годы резко наращивает экспорт магния Китай. В России одним из крупнейших производителей магния являются титано-магниевый комбинат в г.Березники (Пермская обл.) и Соликамский магниевый завод. Производство магния разворачивается также в г. Асбест.
Магний – самый легкий конструкционный материал, используемый в промышленных масштабах. Его плотность (1,7 г см–3) составляет менее двух третей плотности алюминия. Сплавы магния весят вчетверо меньше стали. Кроме того, магний прекрасно обрабатывается и может быть отлит и переделан любыми стандартными методами металлообработки (прокатка, штамповка, волочение, ковка, сварка, пайка, клепка). Поэтому его основная область применения – в качестве легкого конструкционного металла.
Магниевые сплавы обычно содержат более 90% магния, а также 2–9% алюминия, 1–3% цинка и 0,2–1% марганца. Сохранение прочности при высокой температуре (до 450° С) заметно улучшается при сплавлении с редкоземельными металлами (например, празеодимом и неодимом) или торием. Эти сплавы можно использовать для корпусов автомобильных двигателей, а также фюзеляжей и шасси самолетов. Магний применяют не только в авиации, но и для изготовления лестниц, мостков в доках, грузовых платформ, транспортеров и подъемников, а также в производстве фотографического и оптического оборудования.
В промышленный алюминий добавляют до 5% магния для улучшения механических свойств, свариваемости и устойчивости к коррозии. Магний также применяют для катодной защиты других металлов от коррозии, как поглотитель кислорода и восстановитель при производстве бериллия, титана, циркония, гафния и урана. Смеси порошка магния с окислителями используют в пиротехнике для приготовления осветительных и зажигательных составов.
Соединения магния.
Преобладающая степень окисления (+2) для магния обусловлена его электронной конфигурацией, энергиями ионизации и размерами атома. Степень окисления (+3) невозможна, так как третья энергия ионизации составляет для магния 7733 кДж моль–1. Эта энергия гораздо выше, чем можно компенсировать образованием дополнительных связей, даже если они будут преимущественно ковалентными. Причины неустойчивости соединений магния в степени окисления (+1) менее очевидны. Оценка энтальпии образования таких соединений показывает, что они должны быть устойчивыми по отношению к составляющим их элементам. Причиной того, что соединения магния(I) не устойчивы, является гораздо более высокое значение энтальпии образования соединений магния(II), что должно привести к быстрому и полному диспропорционированию:
Mg(к) + Cl2(г) = MgCl2(к);
DН°обр = –642 кДж/(моль MgCl2)
2Mg(к) + Cl2(г) = 2MgCl(к);
DН°обр = –250 кДж/(2 моль MgCl)
2MgCl(к) = Mg(к) + MgCl2(к);
DН°диспроп = –392 кДж/(2 моль MgCl)
Если будет найден путь синтеза, который затруднит диспропорционирование, такие соединения, возможно, будут получены. Имеются некоторые доказательства образование частиц магния(I) при электролизе на магниевых электродах. Так, при электролизе NaCl на магниевом аноде выделяется водород, а количество магния, потерянное анодом, соответствует заряду +1,3. Аналогично при электролизе водного раствора Na2SO4 количество выделившегося водорода соответствует окислению воды ионами магния, заряд которых соответствует +1,4.
Большинство солей магния хорошо растворяются в воде. Процесс растворения сопровождается незначительным гидролизом. Полученные растворы имеют слабокислотную среду:
[Mg(H2O)6]2+ + H2O  [Mg(H2O)5(OH)]+ + H3O+
[Mg(H2O)5(OH)]+ + H3O+
Соединения магния со многими неметаллами, в том числе с углеродом, азотом, фосфором, серой необратимо гидролизуются водой.
Гидрид магния состава МgН2 представляет собой полимер с мостиковыми атомами водорода. Координационное число магния в нем равно 4. Такое строение приводит к резкому снижению термической устойчивости соединения. Гидрид магния легко окисляется кислородом воздуха и водой. Эти реакции сопровождаются большим выделением энергии.
Нитрид магния Mg3N2. Образует желтоватые кристаллы. При гидролизе нитрида магния образуется гидрат аммиака:
Mg3N2 + 8H2O = 3Mg(OH)2 + 2NH3·H2O
Если гидролиз нитрида магния проводить в щелочной среде, гидрат аммиака не образуется, а выделяется газообразный аммиак. Гидролиз в кислотной среде приводит к образованию катионов магния и аммония:
Mg3N2 + 8H3O+ = 3Mg2+ + 2NH4+ + 8H2O
Магния оксид MgO называют жженой магнезией. Его получают обжигом магнезита, доломита, основного карбоната магния, гидроксида магния, а также прокаливанием бишофита MgCl2·6H2O в атмосфере водяного пара.
Реакционная способность оксида магния зависит от температуры его получения. Оксид магния, приготовленный при 500–700° С, называют легкой магнезией. Он легко реагирует с разбавленными кислотами и водой с образованием соответствующих солей или гидроксида магния, поглощает диоксид углерода и влагу из воздуха. Оксид магния, полученный при 1200–1600° С носит название тяжелой магнезии. Он характеризуется кислотостойкостью и водостойкостью.
Оксид магния широко используется как жаростойкий материал. Он отличается одновременно высокой теплопроводностью и хорошими электроизолирующими свойствами. Поэтому это соединение применяется в изолирующих радиаторах для местного нагрева.
Более легкие сорта магнезий используют для приготовления магнезиального цемента и строительных материалов на его основе, а также в качестве вулканизирующего агента в резиновой промышленности.
Гидроксид магния Mg(OH)2 образует бесцветные кристаллы. Растворимость этого соединения невелика (2·10–4 моль/л при 20° С). Его можно перевести в раствор действием солей аммония:
Mg(OH)2 + 2NH4Cl = MgCl2 + 2NH3·H2O
Гидроксид магния термически неустойчив и при нагревании разлагается:
Mg(OH)2 = MgO + H2O
В промышленных масштабах гидроксид магния получают осаждением известью из морской воды и природных рассолов.
Гидроксид магния является мягким основанием, которое в виде водного раствора (магнезиальное молоко) широко используется для снижения кислотности желудочного сока. При этом, несмотря на мягкость, Mg(OH)2 нейтрализует кислоты в 1,37 раз больше, чем гидроксид натрия NaOH и в 2,85 раз больше, чем гидрокарбонат натрия NaHCO3.
Его используют также для получения оксида магния, рафинирования сахара, очистки воды в котельных установках, в качестве компонента зубных паст.
Карбонат магния MgCO3 образует бесцветные кристаллы. Он встречается в природе в безводном виде (магнезит). Кроме того, известны пента-, три- и моногидраты карбоната магния.
Растворимость карбоната магния в отсутствие диоксида углерода составляет около 0,5 мг/л. В присутствии избытка диоксида углерода и воды карбонат магния переходит в растворимый гидрокарбонат, а при кипячении происходит обратный процесс. С кислотами карбонат и гидрокарбонат взаимодействуют с выделением диоксида углерода и образованием соответствующих солей. При нагревании карбонат магния, не плавясь, разлагается:
MgCO3 = MgO + CO2
Этот процесс используют для получения оксида магния. Кроме того, природный карбонат магния является исходным сырьем для получения металлического магния и его соединений. Его используют также в качестве удобрений и для снижения кислотности почв.
Рыхлый порошок карбоната магния засыпают между двойными стенками хранилищ для жидкого кислорода. Эта теплоизоляция дешева и надежна.
Сульфат магния MgSO4 известен в безводном состоянии, а также в виде различных гидратов. В природе встречаются кизерит MgSO4·H2O, эпсомит MgSO4·7H2O и гексагидрат MgSO4·6H2O.
В медицине используется гептагидрат сульфата магния MgSO4·7H2O, широко известный под названиями английская или горькая соль. Это соединение обладает слабительным действием. При внутримышечных или внутривенных вливаниях сульфат магния снимает судорожное состояние, уменьшает спазмы сосудов.
Сульфат магния применяют в текстильной и бумажной промышленности как протраву при крашении, а также в качестве утяжелителя хлопка и шелка и наполнителя бумаги. Он служит сырьем для получения оксида магния.
Нитрат магния Mg(NO3)2 представляют собой бесцветные гигроскопичные кристаллы. Растворимость в воде при 20° С составляет 73,3 г на 100 г. Из водных растворов кристаллизуется гексагидрат. Выше 90° С он обезвоживается до моногидрата. Затем происходит отщепление воды с частичным гидролизом и разложение до оксида магния. Этот процесс используется при синтезе оксида магния особой чистоты. Из нитрата магния получают нитраты других металлов, а также различные соединения магния. Кроме того, нитрат магния входит в состав сложных удобрений и пиротехнических смесей.
Перхлорат магния Mg(ClO4)2 образует очень гигроскопичные бесцветные кристаллы. Он хорошо растворим в воде (99,6 г на 100 г) и органических растворителях. Из водных растворов кристаллизуется гексагидрат. Концентрированные растворы перхлората магния в органических растворителях и его сольваты с молекулами восстановителей взрывоопасны.
Частично гидратированный перхлорат магния, содержащий 2–2,5 молекул воды, выпускают под коммерческим названием «ангидрон». Для получения безводного перхлората магния его сушат в вакууме при 200–300° С. Его используют как осушитель газов. Он поглощает не только пары воды, но и аммиак, пары спиртов, ацетона и других полярных веществ.
Перхлорат магния применяют в качестве катализатора ацилирования по реакции Фриделя – Крафтса, а также как окислитель в микроанализе.
Фторид магния MgF2 мало растворим в воде (0,013 г в 100 г при 25° С). Он встречается в природе в виде минерала селаита. Получают фторид магния взаимодействием сульфата или оксида магния с фтороводородной кислотой или хлорида магния с фторидом калия или аммония.
Фторид магния входит в состав флюсов, стекол, керамики, эмалей, катализаторов, смесей для получения искусственной слюды и асбеста. Кроме того, он является оптическим и лазерным материалом.
Хлорид магния MgCl2 является одной из наиболее промышленно важных солей магния. Его растворимость составляет 54,5 г на 100 г воды при 20° С. Концентрированные водные растворы хлорида магния растворяют оксид магния. Из полученных растворов кристаллизуются MgCl2·mMg(OH)2·nH2O. Эти соединения входят в состав магнезиальных цементов.
Хлорид магния образует кристаллогидраты с 1, 2, 4, 6, 8 и 12 молекулами воды. С ростом температуры число молекул кристаллизационной воды уменьшается.
В природе хлорид магния встречается в виде минералов бишофита MgCl2·6H2O, хлормагнезита MgCl2, а также карналлита. Он содержится в морской воде, рапе соляных озер, некоторых подземных рассолах.
Безводный хлорид магния используют в производстве металлического магния и оксида магния, гексагидрат – для получения магнезиальных цементов. Водный раствор хлорида магния применяют как хладагент и антифриз. Он служит средством против обледенения летных полей аэродромов, железнодорожных рельсов и стрелок, а также против смерзания угля и руд. Раствором хлорида магния пропитывают древесину для придания ей огнестойкости.
Бромид магния MgBr2 хорошо растворим в воде (101,5 г на 100 г при 20° С). Из водных растворов кристаллизуется от –42,7 до 0,83° С в виде декагидрата, при более высокой температуре – в виде гексагидрата. Он образует многочисленные кристаллосольваты, такие как MgB2·6ROH (R = Me, Et, Pr), MgBr2·6Me2CO, MgBr2·3Et2O, а также аммины MgBr2·nNH3 (n = 2–6).
Комплексные соединения магния. В водных растворах ион магния существует в виде аквакомплекса [Mg(H2O)6]2+. В неводных растворителя, например в жидком аммиаке, ион магния образует комплексы с молекулами растворителя. Из таких растворов обычно кристаллизуются сольваты солей магния. Известно несколько галогенидных комплексов типа MX42–, где Х – галогенид-анион.
Среди комплексных соединений магния особое значение имеют хлорофиллы, являющиеся модифицированными порфириновыми комплексами магния. Они являются жизненно важными для фотосинтеза в зеленых растениях.
Магнийорганические соединения. Для магния получены многочисленные соединения, содержащие связи металл – углерод. Особенно много исследований посвящено реактивам Гриньяра RMgX (X = Cl, Br, I).
Реактивы Гриньяра – самые важные металлоорганические соединения магния и, вероятно, наиболее используемые металлоорганические реагенты. Это связано с легкостью их получения и синтетической разносторонности. Установлено, что в растворе эти соединения могут содержать разнообразные химические частицы, находящиеся в подвижном равновесии.
Реактивы Гриньяра обычно получают медленным добавлением органического галогенида к взвеси магниевых стружек в соответствующем растворителе при интенсивном перемешивании и полном отсутствии воздуха и влаги. Реакция обычно начинается медленно. Она может быть инициирована маленьким кристалликом иода, который разрушает защитный слой на поверхности металла.
Реактивы Гриньяра широко применяются для синтеза спиртов, альдегидов, кетонов, карбоновых кислот, эфиров и амидов и, вероятно, являются самыми важными реагентами для создания связей углерод–углерод, а также связей между атомами углерода и других элементов (азот, кислород, сера и т.д.).
Соединения R2Mg обычно разлагаются при нагревании. В кристаллическом состоянии они имеют структуру линейных полимеров с мостиковыми алкильными группами. Соединение MgMe2 представляет собой нелетучий полимер, устойчивый до ~250° С, не растворимый в углеводородах и лишь немного растворимый в эфире. Соединение MgEt2 и более высокие гомологи очень похожи на MgMe2, но они разлагаются при более низкой температуре (175–200° С), образуя соответствующий алкен и MgH2 по реакции, обратной их получению. Похож на них и MgPh2; он не растворим в бензоле, растворяется в эфире с образованием мономерного комплекса MgPh2·2Et2O и разлагается при 280° С с образованием Ph2 и металлического магния.
Биологическая роль магния.
Зеленые листья растений содержат хлорофиллы, которые представляют собой магнийсодержащие порфириновые комплексы, участвующие в фотосинтезе.
Магний также тесно вовлечен в биохимические процессы в организмах животных. Ионы магния необходимы для инициирования ферментов, отвечающих за превращения фосфатов, для переноса нервного импульса и для метаболизма углеводов. Они также участвуют в сокращении мышц, которое инициируется ионами кальция.
Несколько лет назад ученые Миннесотского университета в США установили, что яичная скорлупа тем прочнее, чем больше она содержит магния.
В организме взрослого человека массой 65 кг содержится около 20 г магния (в основном, в виде ионов). Большая его часть сосредоточена в костях. Во внутриклеточной жидкости присутствуют комплексы магния с АТФ и AДФ.
Суточная потребность в этом элементе составляет 0,35 г. При однообразном питании, нехватке зеленых овощей и фруктов, а также при алкоголизме нередко возникает дефицит магния. Особенно богаты магнием абрикосы, персики и цветная капуста. Есть он и в обычной капусте, картофеле, помидорах.
Статистика утверждает, что у жителей районов с более теплым климатом спазмы кровеносных сосудов случаются реже, чем у северян. Считают, что причиной этого являются особенности питания в холодных краях. Они едят меньше фруктов и овощей, а, значит, получают меньшее количество магния.
Исследования французских биологов показали, что в крови уставших людей содержится меньше магния, чем у отдохнувших. Считают, что диета, богатая магнием должна помочь медикам в борьбе с таким серьезным недугом, как переутомление.
Елена Савинкина
Greenwood N.N., Earnshaw A. Chemistry of the Elements, Oxford: Butterworth, 1997
Кольман Я., Рём К.-Г. Наглядная биохимия: Пер. с нем. М., Мир, 2000
Ответь на вопросы викторины «Неизвестные подробности»
