РАДИЙ
РАДИЙ – радиоактивный химический элемент II группы периодической системы, аналог бария; относится к щелочноземельным элементам. Стабильных изотопов не имеет; наиболее долгоживущие – 226Ra (период полураспада t1/2 = 1600 лет) и 228Ra (t1/2 = 5,75 года). Остальные изотопы (всего их известно 25) «живут» значительно меньше, некоторые – доли секунды; почти все они получены искусственно.
Радий в природе и его свойства.
Несмотря на сравнительно малое время жизни по сравнению с возрастом Земли (около пяти миллиардов лет), некоторые изотопы радия, хотя и в очень малых количествах, встречаются в природе. Происходит это благодаря существованию в природе трех радиоактивных рядов, в которых изотопы радия непрерывно образуются при распаде долгоживущих (так называемых материнских) радионуклидов: урана-238 (из него получается 226Ra), урана-235 (он дает 223Ra, t1/2 = 11,4 суток) и тория-232 (дает 228Ra и 224Ra, t1/2 = 3,7 суток). Очевидно, что чем меньше период полураспада данного радионуклида, тем меньше его содержание в минералах, даже самый долгоживущий, 226Ra, содержится в земной коре в количестве всего одной десятимиллиардной доли процента, обычно в тех же породах, в которых содержится уран.
Чистый радий – блестящий серебристо-белый металл, быстро тускнеющий на воздухе из-за образования на его поверхности оксида и нитрида. С водой реагирует более энергично, чем барий, выделяя водород. Плавится радий при 969° С, кипит при 1507° С, плотность – около 6 г/см3. Любые физические и химические свойства радия изучать трудно из-за его очень высокой радиоактивности. Радий непрерывно выделяет теплоту, и если нет условий для теплоотвода, металл быстро нагревается и может даже расплавиться. Продукт распада радия – радиоактивный газ радон. Радий вместе с продуктами своего распада излучает все три вида радиации – a-, b- и g-лучи. Из-за высокой радиоактивности радий и его соединения светятся в темноте, его бесцветные соли быстро желтеют, а затем приобретают коричневую, вплоть до черной, окраску; их водные растворы разлагают воду, выделяя из нее водород и кислород.
Если не считать сильной радиоактивности, химические свойства радия и его соединений мало отличаются от аналогичных свойств бария. Как и у бария, легко растворимы хлорид, бромид, иодид, нитрат радия, а фторид, карбонат и сульфат почти нерастворимы. Гидроксид Ra(OH)2 – сильная щелочь.
В поисках новых радиоактивных элементов.
Радий неотделим от имени открывших его супругов Кюри, которые посвятили его поискам, выделению и изучению свойств многие годы. Открытые в 1896 А.Беккерелем «урановые лучи» заинтересовали многих ученых, среди них были французский физик Пьер Кюри и его жена Мария Склодовская-Кюри.
Если Беккереля в основном волновали свойства «урановых лучей» и источник их энергии, то Кюри, будучи скорее химиком, задалась вопросом, является ли уран уникальным в этом отношении и нет ли других элементов с подобными свойствами Нужно было научиться точно измерять степень радиации. Сейчас такой вопрос решается просто с помощью приборов, например, счетчиков Гейгера, но они появились только в 1908, а фотопластинки были слишком грубым инструментом и требовали много времени для экспозиции и последующего проявления. Скорость опадания золотых листочков электроскопа тоже зависела от многих невоспроизводимых факторов. П.Кюри сконструировал электрометр, позволяющий точно измерять очень малые токи, измеряемые триллионными долями ампера – пикоамперами (пА). В приборе использовался открытый им вместе с братом Жаком пьезоэлектрический эффект – появление на гранях некоторых кристаллов при их сдавливании электрических зарядов (этот эффект используется, например, в кварцевых часах, в пьезозажигалках). Точно дозируя давление на кристалл, можно было компенсировать и, таким образом, измерять очень малые токи. Конструкция состояла из двух расположенных горизонтально с небольшим зазором металлических дисков, на которые подавалось напряжение около 100 В. Если между дисками находился только слой воздуха, тока не было, но если на нижний диск насыпали тонким слоем определенное количество какого-либо соединения урана, воздух благодаря ионизации под действием «урановых лучей» становился проводником, при этом между дисками протекал очень слабый ток, который можно было измерить и таким образом количественно и довольно точно определить мощность излучения.
Используя этот метод, Кюри начала тестировать одно вещество за другим – все, которые она только могла достать, одолжить в химических лабораториях, выпросить в минералогических музеях (она не только аккуратно возвратила образцы владельцам, но и выразила им благодарность в своей публикации). Из всех веществ, не содержащих уран, активность проявили только соединения тория.
Аналогичными исследованиями занимались и другие ученые. Одновременно и независимо от нее радиоактивность тория обнаружил немецкий физик Герхард Карл Шмидт (1865–1949). Это неудивительно: торий и уран были последними, самыми тяжелыми, элементами в таблице Менделеева тех времен, поэтому от них можно было ждать всяких неожиданностей. Об этом написал в последнем прижизненном издании (1906) своего учебника Основы химии и сам Менделеев: «Наивысшая, из известных, концентрация массы весомого вещества в неделимую массу атома, существующая в уране, уже a priori должна влечь за собою выдающиеся особенности».
Неожиданными оказались количественные результаты измерений. Так, взятый у Муассана металлический уран (он был получен восстановлением оксида углем и содержал примесь углерода) дал ток 23–24 пА; природный монацит (смешанный фосфат редких земель и тория) – 5 пА; чрезвычайно редкий минерал самарскит (смесь оксидов редкоземельных элементов, U, Fe, Nb, Ta и Ti) – 11 пА; черный торит ThSiO4 (обычно содержит примесь урана) – 14 пА, а прозрачные оранжевые кристаллы оранжита (невыветренный силикат тория) – 20 пА; черный оксид урана U2O5 – 27 пА; урановая смоляная руда (урановая смолка) из разных источников (она образует минералы уранинит или настуран примерного состава UO2) – от 16 до 83 пА; желтый минерал отенит Ca(UO2)2(PO4)2·(10–12)H2O – 27 пА; редкий природный минерал хальколит (торбернит) красивого зеленого цвета Cu(UO2)2(PO4)2·(8–12)H2O – 52 пА; желтый минерал карнотит K2(UO2)2V2O8·3H2O – 62 пА.
Результаты не соответствовали содержанию в минералах известных радиоактивных элементов – урана и тория. Так, хальколит, в котором масса урана составляет лишь около 50%, оказался вдвое активнее, чем чистый уран, синтезированный собственноручно М.Кюри искусственный хальколит (двойной фосфат меди – уранила) показал небольшую активность, которая приблизительно соответствовала содержанию в этой соли урана. Стало ясно, что в природных минералах, которые проявили наибольшую активность, содержится, помимо урана, какой-то другой, неизвестный элемент. «Активность этих минералов не представляла бы ничего удивительного, – записала Мария в лабораторном журнале, – если бы была пропорциональна количеству содержащегося в них урана или тория. Но это было не так. Некоторые из этих минералов проявили активность в три или четыре раза большую, чем надлежало по расчету для урана. Я тщательно проверила этот поразительный факт и не могла больше сомневаться в его правильности... Аномальная активность хальколита, обусловлена не его химическим составом; минерал, конечно, содержит в слабой пропорции элемент более активный, чем уран...». Не последнюю роль, возможно, сыграла и «подсказка» самого Беккереля: когда-то в беседе с Пьером Кюри он высказал предположение о том, что обнаруженная им радиоактивность урана может быть связана с какими-то очень активными примесями в этом элементе.
Все известные элементы были уже изучены и не обладали нужным свойством. Химический анализ радиоактивных минералов соответствовал их формуле, это означало, что нового элемента в этих минералах исключительно мало, поэтому этот элемент (возможно, не он один) быть очень активным! Как только стало ясно, что в урановых и ториевых рудах содержится неизвестное вещество с очень высокой радиоактивностью, началась работа по его выделению. Завершилась она выдающимся открытием новых химических элементов – полония и радия.
Впоследствии Кюри писала по этому поводу: «Я назвала радиоактивностью способность испускать такие лучи и создала новый термин, принятый с тех пор в науке». На латыни radius – палочка, спица в колесе, а также радиус круга и луч; radiare – испускать лучи, сиять; в английском слово radiant (излучающий) появилось еще в 15 в., т.е. термин, введенный Кюри, должен был означать самопроизвольное («активное») излучение некоторыми веществами.
Стало ясно, что в урановой смолке присутствует неизвестный радиоактивный элемент (или несколько элементов). Тщательный химический анализ этого вещества привел в 1898 к открытию нового радиоактивного элемента – полония.
В первом исследовании урановой смолки супруги Кюри упустили важное обстоятельство. Оказалось, что если из азотнокислого раствора осадить сульфат бария (потом его перевели в растворимый хлорид), он обнаруживает радиоактивность. Стало очевидным, что это еще один радиоактивный элемент – на этот раз аналог не висмута, а бария. Для того чтобы сконцентрировать этот элемент, был использован метод многократной перекристаллизации – тот самый, с помощью которого были разделены очень близкие по свойствам редкоземельные элементы. В данном случае он был основан на разной растворимости солей бария и радия. Так, в 100 г воды при 20° С растворяется 35,7 г хлорида бария, а хлорида радия – почти в два раза меньше, поэтому если из раствора выделить в осадок 1/3 хлорида бария, то хлорида радия выделится 2/3. По этому методу (он называется фракционной кристаллизацией) раствор хлоридов частично выпаривают до образования кристаллов, в которых доля радия выше, чем в растворе. Эти кристаллы снова растворяют и повторяют все сначала. Таким образом, доля радия в выпадающих кристаллах постепенно растет. Раствор, обедненный радием, не выбрасывают, а подвергают дробной кристаллизации. Кроме бария и радия (и урана) исходный минерал содержал довольно много свинца, кремния, тантала, протактиния, железа, тория, актиния, полония, и все эти элементы следовало предварительно отделить от бария (с ничтожной примесью радия). Этот метод требует очень большого числа операций, но другого способа выделить новый элемент не было. На каждой стадии соответствующую фракцию с помощью электрометра проверяли на радиоактивность и таким образом контролировали степень обогащения.
Постепенно супруги Кюри (с помощью Бемона) получили препарат бария, который был в 60 раз активнее, чем чистый уран, после еще нескольких перекристаллизаций – уже в 900 раз более активный, Но опыты пришлось прекратить: последняя, самая активная, фракция была такой маленькой, что дальше работать с ней было уже невозможно – для выделения нового элемента нужны были не граммы, и даже не килограммы руды, а тонны.
26 декабря 1898 была опубликована статья Мосье Пьера Кюри, мадам П. Кюри и мосье Г.Бемона, О новом сильно радиоактивном веществе, содержащемся в урановой смолке, в которой сообщалось, что был исследован спектр обогащенного препарата, который был в 60 раз активнее урана, и в нем обнаружена едва заметная новая линия в ультрафиолетовой области (длина волны 381 нм), эта же линия была отчетливо видна в последнем образце, в 900 раз более активном, чем уран. Интенсивность спектральной полосы была пропорциональна радиоактивности препаратов, что служило хорошим доводом приписать ее новому радиоактивному элементу. Его решили назвать радием. Попытки определить атомную массу нового элемента (без этого химики не признали бы его за новый элемент, а не радиоактивный изотоп бария) дали значение, почти не отличающееся от бария. Вывод в статье был однозначным: «В новом веществе все еще очень велико содержание бария. Поэтому радиоактивность радия должна быть огромной».
С этой радиоактивностью не все было в порядке. Так, 13 июля 1899 П.Кюри отметил в лабораторном журнале непонятный факт – препарат сульфата радия, активность которого в начале года составляла от 150 до 200 единиц, в середине июля показывал уже 600. На той же странице – аналогичная запись М.Кюри – карбонат радия с активностью 1200 вдруг через полгода показал активность 3000. Объяснить это супруги не могли, лишь впоследствии из работ Резерфорда стало известно, что из радия образуются другие короткоживущие радиоактивные элементы, так что только a-активность радия должна примерно через три недели увеличиться вчетверо. Но при одном условии: препарат должен находиться в закрытом сосуде, так как первый продукт превращения радия – газообразный радон.
Определение атомной массы даже самого активного препарата давало значение, мало отличающееся от атомной массы бария (137). Это означало, что концентрация радия в урановой смолке очень мала. Значит, для выделения нового элемента нужно будет переработать очень много дорогого минерала, которого у них в нужном количестве не было, и сколько его потребуется, не знал никто. В статье от 26 декабря было примечание, в котором говорилось, что «профессор Венского университета мосье Зюсс любезно согласился уговорить австрийское правительство выслать в Париж 100 кг отходов от переработки урановой смолки на шахтах Иоахимсталя».
Как выяснилось, и 100 кг было мало. Урановую смолку добывали в Богемии (латинизированное название Чехии), вблизи знаменитых шахт Иоахимсталя (ныне – город в Чехии Яхимов). Урановую руду сплавляли с содой при доступе воздуха. Плав обрабатывали сначала водой – уран при этом переходил в раствор в виде карбонатного комплекса, затем разбавленной серной кислотой – получался сульфатный комплекс урана. Соединения урана использовали для производства дорогого богемского уранового стекла и глазури по фарфору. Остаток руды после извлечения урана, который содержал весь радий, выбрасывали, и постепенно скопились целые горы отходов, которые сваливали в ближайшем сосновом лесу. Супруги Кюри в конечном счете получили не 100 кг, а более 10 тонн.
Сейчас на стене Парижской Высшей школы физики и химии укреплена памятная доска с надписью: «В 1898 году в лаборатории этой Школы Пьер и Мария Кюри, при помощи Густава Бемона, открыли радий».
Выделение радия.
Работа предстояла огромная – химическая переработка (вручную) многих тонн материала; она заняла четыре года. Вначале остатки кипятили с большим избытком концентрированного раствора соды – при этом содержащиеся в них не растворимые ни в воде, ни в кислотах сульфаты бария и радия (и частично кальция) переходили в карбонаты: Ba(Ra)SO4 + Na2CO3 ® Ba(Ra)CO3 + Na2SO4. Раствор Na2SO4 сливали, а осадок карбонатов бария и радия уже легко растворялся в разбавленной соляной кислоте: Ba(Ra)CO3 + 2HCl ® Ba(Ra)Cl2 + CO2 + H2O. Раствор отфильтровывали от примесей и добавлением серной кислоты из него снова выделяли сульфаты кальция, бария и радия – их получалось от 10 до 20 кг из тонны исходного вещества. Затем весь цикл повторяли, пока не получались чистые соли бария и радия (примерно 8 кг из тонны), отделенные от более растворимого кальция. Использовали и другие химические приемы, необходимые для отделения радия от следов других радиоактивных элементов. Так, свинец, висмут и сопровождающий его полоний осаждали сероводородом в виде нерастворимых сульфидов. Актиний осаждался вместе с железом, алюминием и редкоземельными элементами с помощью раствора аммиака. Затем методом дробной кристаллизации выделяли все более чистую соль радия. По мере увеличения доли радия выпадающие вначале бесцветные кристаллы со временем под действием собственного излучения желтели, затем становились оранжевыми или розовыми, а после растворения снова дали бесцветный раствор.
Сама Кюри много лет спустя призналась, что не уверена, проявила ли бы она такую настойчивость, если бы знала, как мало радия содержится в руде и какая титаническая работа предстоит для получения хотя бы мизерного его количества. Для работы директор Школы выделил им старый сарай с застекленной крышей, где раньше была прозекторская. По подсчетам австрийского физика Стефана Мейера (1872–1950) М.Кюри пришлось переработать вручную свыше 11 тонн отходов, неудивительно, что к вечеру она буквально падала от усталости. Тем не менее, впоследствии она признавалась, что именно в этом сарае провела свои лучшие и счастливейшие годы.
Затем появились помощники и работа пошла быстрее.Весной 1902, после переработки тонны урановых отходов, масса радия (в виде RaCl2) достигла 0,1 г. Позднее подсчитали, что тонна урановой смолки теоретически содержит 0,17 г радия в виде хлорида. Таким образом, потери оказались сравнительно невелики, если учесть колоссальный объем работы в неподходящих условиях и исключительно малое содержание радия в руде: 34 миллионные доли процента. Это и позволило В.Маяковскому написать известные строчки:
Поэзия –
та же добыча радия.
В грамм добыча,
в год труды.
Изводишь,
единого слова ради,
Тысячи тонн
словесной руды.
Чистота препарата была подтверждена Демарсе с помощью спектрального анализа. Полученного вещества было достаточно, чтобы определить атомную массу радия традиционным методом: точную навеску RaCl2 растворяли, осаждали нитратом серебра нерастворимый AgCl, который высушивали и взвешивали. Получилось 225 – именно это значение стояло на месте предполагаемого, еще не открытого элемента в таблице, помещенной Менделеевым в первом издании своего учебника Основы химии.
После переработки восьми тонн у М.Кюри был уже целый грамм радия. Активность нового элемента оказалась в миллион (!) раз выше, чем у урана. Под действием его излучения светились алмазы, а бумага и хлопчатобумажная ткань разрушались, на коже появлялись ожоги, а потом язвы. Необычные свойства нового элемента требовали все больших его количеств. К концу 1903 Кюри имели уже 10 тонн отходов из 20, зарезервированных для них при содействии Венской академии наук. Возросли и расходы на доставку – их оплатил банкир Эдмонд Ротшильд. Исходного сырья стало так много, что обработать его в сарае было уже невозможно. Пьер Кюри организовал первоначальную обработку отходов на химическом заводе в Ножан-на-Марне – небольшом городке к востоку от Парижа. На нем использовали несколько упрощенную методику Марии Кюри, а дробную кристаллизацию осуществляли не с хлоридами, а с бромидами бария и радия (для них коэффициент разделения оказался выше). Промышленную добычу радия консультировали супруги Кюри и их друг и коллега французский физикохимик Андре Луи Дебьерн (1874–1949), который в 1899 открыл в урановой смолке еще один радиоактивный элемент – актиний. Финансовую помощь пришла из нескольких источников (среди них были и анонимные). Французская академия наук предоставила грант в 20 000 франков (около 4000 долл.). Когда в других странах также начались работы по добыче радия, супруги Кюри могли заработать намного больше, чем получили за Нобелевскую премию. Однако они отказались взять патент на свое открытие, хотя цена радия уже достигла 750 тыс. франков за грамм. Кюри безвозмездно снабжала своим радием всех ученых, которые хотели изучать это замечательное вещество. Супруги Кюри убедили Беккереля вернуться к исследованию радиоактивности нового элемента. Он доказал, что сильно отклоняемые магнитным полем b-лучи идентичны «катодным лучам», т.е. представляют собой быстро летящие электроны.
По мере увеличения количества добытого радия стало возможным более подробно исследовать его свойства, а также свойства его соединений. Оказалось, что под влиянием собственного излучения как сами бесцветные соединения радия, так и стеклянные сосуды, в которых они хранятся, со временем темнеют. Все соединения радия в темноте испускают голубоватое свечение (светятся возбужденные атомы азота).
Пьер и Мария Кюри обнаружили потемнение стекла под влиянием излучения радия (сейчас стекла для очков тонируются тоже с помощью радиации). Немецкий физик Ф.О.Гизель обнаружил, что лучи радия окрашивают и природные кристаллы каменной соли (NaCl) и плавикового шпата (CaF2). Он же показал, что RaBr2 окрашивает пламя в карминовый цвет (как стронций), а в спектре радия есть линии в красной, сине-зеленой и фиолетовой областях спектра.
В 1904 Пьер Кюри в Королевском институте в Лондоне продемонстрировал, как писали английские ученые, «поразительный эксперимент». Ему помогал английский физик и химик Джеймс Дьюар (1842–1923), который в 1898 впервые получил большое количество жидкого водорода и изобрел «сосуды Дьюара» для хранения сжиженных газов (в быту их называют «термосами»). Эксперимент показывал, что излучение радия и выделяемая им теплота не меняются при охлаждении до температуры жидкого воздуха (около –190° С) и даже жидкого водорода (–252,8° С). Измерения показали, что сам радий (за счет a-излучения) выделяет в час более 105 Дж/г, а радий вместе с продуктами его распада – почти 590 Дж/ч, причем на долю a-частиц приходится около 89%, на долю b-частиц – 4,5%, остальное дает g-излучение.
В 1910 М.Кюри и Дебьерн впервые получили металлический радий. Они использовали метод, примененный ранее для выделения бария. Для этого водный раствор RaCl2 был подвергнут электролизу с ртутным катодом и платино-иридиевым анодом. Образовавшуюся на катоде амальгаму радия нагревали в потоке водорода, постепенно повышая температуру до 700° С (почти до плавления радия), чтобы отогнать ртуть (она кипит при 357° С).
На Международном конгрессе по радиоактивности и электричеству, собравшемся в Брюсселе в 1910, М.Кюри была поручена подготовка международного эталона радия; он был нужен в качестве стандарта радиоактивности. Несмотря на заметное ухудшение здоровья (помимо переутомления, начала сказываться лучевая болезнь, о которой в то время ничего не знали и потому не предпринимали никаких мер безопасности), Мария приготовила эталон в течение одного месяца. В последующие годы на основании этого эталона были изготовлены многочисленные вторичные эталоны, которые были переданы в Австрию, Германию, Англию, Францию, США, Канаду, Швецию, Японию, Португалию, Данию, Бельгию, Чехословакию, Венгрию, СССР, Австралию Конгресс, свидетельству английских физиков, дал название единице радиоактивности «кюри» в честь Марии Кюри. Однако сама Мария писала, что «конгресс пожелал дать этой единице название кюри, чтобы почтить память Пьера Кюри и его труды в области радиоактивности».
В ноябре 1911 года впервые Нобелевская премия была вручена повторно. Как было отмечено в протокольном решении Шведской академии наук, премия по химии присуждалась «Марии Склодовской-Кюри в знак признания ее вклада в развитие химии, который она внесла открытием радия и полония, определением свойств радия и выделением радия в металлической форме, и, наконец, за ее эксперименты с этим элементом».
«Радиевый бум».
Отказ супругов Кюри на извлечение материальных выгод из своего открытия открыл дорогу к получению и применению радия для ученых всех стран. Начали выходить специальные журналы, посвященные радию и радиоактивности. В 1913 осуществилась мечта Пьера Кюри – в Париже был организован Институт радия. Руководителем одной из двух его лабораторий была Мария Кюри. В том же году был основан Национальный институт радия в США. Еще раньше, в 1910, Институт радия открылся в Вене, его директором был назначен Стефан Мейер. В 1913 лаборатория по радиоактивности открылась в Варшаве. В 1932 при активной помощи сестры Марии Брониславы был создан варшавский Институт радия (ныне – Онкологический институт имени Марии Склодовской-Кюри). В 1922 Радиевый институт был основан в Петрограде; его директором стал В.И.Вернадский (1863–1945). За год до этого в нашей стране первые препараты радия из отечественной ферганской руды получили радиохимик Виталий Григорьевич Хлопин (в будущем – академик и директор Института) и физикохимик и металлург Иван Яковлевич Башилов (1892–1953), предложивший технологию извлечения радия, урана и ванадия (эти элементы содержатся в минерале карнотите).
Когда выяснилась возможность использования радия в медицине, в мире развернулась настоящая «радиевая лихорадка». На всех континентах интенсивно велся поиск и добыча радиоактивных урановых руд, из которых радий добывали в основном по методу М.Кюри.
Цена на радий начала стремительно расти и вскоре значительно превысила стоимость алмазов (в середине 1910-х – почти 180 тыс. долл. за грамм). При тогдашней цене золота (35 долл. за унцию) 1 г радия стоил столько же, сколько 160 кг золота.
Резкое подорожание радия в начале века было связано также с тем, что в конце 1903 австрийское правительство наложило эмбарго на вывоз из Иоахимсталя как самой урановой руды, так и остатков от ее переработки и вскоре само построило там завод по добыче радия. К 1910 на нем получили уже 13 граммов радия, и до 1922 этот завод оставался европейским лидером по производству радия. Огромная цена радия стимулировала поиск его руд и добычу на всех континентах. В 1920–1930-е один за другим открывались новые предприятия по переработке урановых руд и добыче радия – как на своем сырье, так и на привозном. Завод в Ножане, организованный еще Пьером Кюри, работал на разнообразном сырье: урановую смолку ввозили из Венгрии, Швеции, Канады и Колорадо, отенит добывался в самой Франции, а также привозился из Португалии, хальколит – из Богемии, карнотит – из Португалии и Юты (США), а торианит (содержащий уран ThO2) – даже из Цейлона. Добывали торианит и в Японии. В Лондоне перерабатывали руду, добываемую на шахтах юго-западной оконечности Англии (полуостров Корнуолл), часть этой руды перевозили также на переработку во Францию. На заводе близ Стокгольма радий добывали из собственных урансодержащих сланцев и урановой смолки из Норвегии (которая в 1905 стала независимой). В Австралии радий получали из руд, найденных в южных пустынях...
Россия включилась в гонку в 1910, переработку вела частная компания в Фергане, хотя руда оказалась довольно бедной. Во время войны работа прекратилась, но после революции был построен уже государственный завод на Каме, а в 1931 – еще один в Москве. Есть и позорные страницы в отечественной истории радия. Еще в 1930-е малограмотный горнорабочий И.Г.Прохоров начал рассказывать и писать в высокие партийные инстанции о своей мифической встрече в 1914 в Восточной Сибири с Марией Кюри, которая якобы лично подтвердила наличие богатых радиево-урановых месторождений в Минусинском уезде Енисейской губернии. Этот рассказ (вошедший даже в серьезные научные сборники) впоследствии был использован органами госбезопасности СССР для массовых репрессий против советских геологов в 1949 под предлогом сокрытия ими радиево-урановых месторождений.
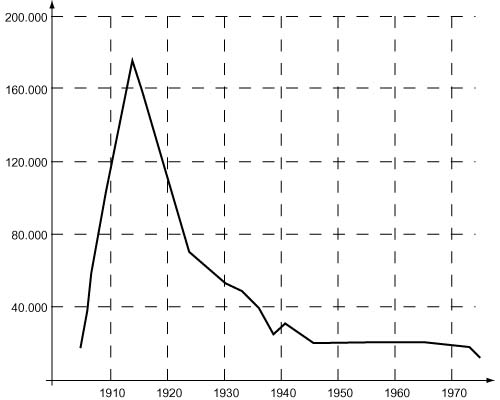
С 1913 по 1922 основным поставщиком радия на мировой рынок были США. Радий там добывался в штате Колорадо, а его извлечением занималось несколько компаний, лидером была «Стандард Кемикл», которая извлекала радий из карнотитовых руд. Пик добычи пришелся на 1921 – 35 г радия, всего же с 1913 по 1923 США получили 196 г радия. Теперь уже уран выбрасывался как ненужный балласт или продавался за бесценок: основной целью был радий.
Но вскоре радиевая промышленность США пришла в упадок: с 1921 начали разрабатываться месторождения в Бельгийском Конго (провинция Катанга), и в 1922 в Бельгии заработал завод близ Антверпена. Африканская руда оказалась очень богатой: она содержала в среднем 50% оксида урана, и если для получения 1 грамма радия в США надо было переработать 300–400 тонн карнотитовой руды, то заводу в Бельгии для того же требовалось всего 10 тонн. С 1922 по 1933 там было выделено 326 г радия. Пик добычи пришелся на конец 1920-х – 60 г радия в год. Но и бельгийцам пришлось сократить производство ввиду сильной конкуренции со стороны Канады. Руду там добывали с 1932 на побережье Большого Медвежьего озера, добыча радия в 1938 достигла 75 г. Данные за последующие годы были засекречены, так как отражали добычу нового стратегического сырья – урана, известно только, что производство радия в Канаде продолжалось до 1954, а в Бельгии – до 1960. С 1930-х весь рынок радия был под контролем бельгийских и канадских компаний. В небольшом количестве радий производили также в Англии, Франции, СССР. В Чехословакии его добывали (в Яхимове) вплоть до 1937.
Общее количество добытого радия увеличивалось быстрыми темпами. Если к 1916 во всем мире было получено 48 г радия, то через 10 лет его было уже 340 г. Постепенное накопление мировых запасов радия, который практически не расходуется (за 10 лет его количество уменьшается за счет распада менее чем на 0,5%), привело к быстрому снижению цены более чем вдвое к началу 1920-х, а затем еще в несколько раз в последующие десятилетия.
Тем не менее, радий оставался очень дорогим элементом. В настоящее время радия накоплено около 3 кг, и больше его практически не добывают. Более того, при переработке урановых руд радий считается вредным побочным продуктом, требующим безопасного захоронения!
Применение радия.
В течение многих десятилетий радий применялся в основном в медицинских целях и лишь в очень малых количествах – для научных исследований. Излучением радия лечили прежде всего злокачественные опухоли, для этого использовали содержащие радий иголки, трубочки или пластинки; их накладывали на больное место или же хирургическим путем вводили на некоторое время прямо в опухоль. Когда цена радия снизилась, в некоторых больницах стали использовать «радиевые пушки» с дистанционным облучением пациентов, они содержали несколько граммов радия. Конечно, не обошлось и без шарлатанов, которые предлагали «чудодейственный радий» от всех недугов – начиная с психических заболеваний и кончая бессонницей. Дошло до продажи «радиевых удобрений», якобы повышающих урожай. В результате некоторые поля в США, Канаде и Франции были «удобрены» радиоактивными веществами.
Широко применялся радий и для получения светящихся составов; с этой целью соли радия смешивали с подходящим люминофором (см. ЛЮМИНЕСЦЕНЦИЯ. СВЕЧЕНИЕ ВЕЩЕСТВ). Такие составы наносили на стрелки часов и компасов, на шкалы военных приборов и даже на предметы быта, не подозревая об опасности. В таких покрытиях обычно использовали сульфид цинка, содержащий от 0,0025 до 0,03% радия. Использовали также способность радия ионизировать воздух и таким образом снимать статический заряд, предотвращая возможность воспламенения горючих паров. В 1930-х в США производились даже ткани из искусственного шелка «с радием», который снимал статическое электричество и предотвращал их слипание. Все это прекратилось, когда стала широко известна опасность радиоактивного облучения и лучевой болезни, более того, после взрыва первых ядерных бомб всеобщее увлечение «радием» и радиацией сменилось прямо противоположной и тоже не всегда обоснованной радиофобией.
Сейчас радий находит лишь ограниченное применение и для этого его накопленных запасов более чем достаточно. В медицине радий иногда используют для кратковременного облучения при лечении злокачественных заболеваний кожи, слизистой оболочки носа, мочеполового тракта. Радий используют и как источник радона для приготовления радоновых ванн. Радий можно использовать и в компактных источниках нейтронов, для этого небольшие его количества помещают в ампулу вместе с бериллием, под действием альфа-излучения (ядер гелия) из бериллия выбиваются нейтроны: 9Be + 4He ® 12C + 1n. Однако сейчас есть множество более дешевых радионуклидов с нужными свойствами, которые получают на ускорителях или ядерных реакторах, например, 60Co (с периодом полураспада t1/2 = 5,3 года), 137Cs (t1/2 = 30,2 года), 182Ta (t1/2 = 115 сут), 192Ir (t1/2 = 74 сут), 198Au (t1/2 = 2,7 сут). В приборах постоянного свечения радий также заменяют теперь тритием (t1/2 = 12,3 года) или 147Pm (t1/2 = 2,6 года).
Радий сильно токсичен; допустимая его концентрация в воздухе исчезающе мала – не более 10 мг/км3 или 10–11 г/м3. При такой концентрации в 1 м3 происходит чуть больше двух распадов атомов радия в секунду. Работа с радием и его препаратами, как и с другими радиоактивными веществами, требует строгого соблюдения защитных мер.
Илья Леенсон
Старосельская-Никитина О.А. История радиоактивности и возникновения ядерной физики. М., 1963
Погодин С.А., Либман Э.П. Как добыли советский радий. М., 1977
Венецкий С.И. О редких и рассеянных. М., 1981
Landa E.R. The First Nuclear Industry. Scientific American, 1982, November
Ответь на вопросы викторины «Неизвестные подробности»